Klíčová slova
inzulínová rezistence • sekrece inzulínu • volné mastné kyseliny • lipotoxicita
Inzulín se uvolňuje z B-buněk pankreatu pulsní sekrecí a krevním oběhem se dostává do cílových tkání, tj. do příčně pruhovaného svalu, tukové tkáně a jater, v nichž po vazbě na specifické receptory uplatňuje svoje metabolické a růstové účinky. Inzulín se váže na alfa-podjednotku receptoru, což je signálem pro autofosforylaci beta-podjednotky, jejíž nitrobuněčná doména má charakter tyrozinkinázy. Aktivace receptoru je pak signálem pro autofosforylačně-defosforylační reakce, které probíhají dvěma kaskádami. První je zprostředkována přes substrát inzulínového receptoru (IRS), na nějž se přenáší signál z aktivovaného receptoru. Tato molekula funguje jako druhý posel. Aktivace IRS vyvolá následně stimulaci fosfatidylinositol-3-kinázy (PI-3-K), zprostředkující metabolické efekty inzulínu. Výsledkem jsou metabolické účinky inzulínu, které se vyznačují ukládáním glukózy ve formě glykogenu (stimulací glykogensyntázy) a ukládáním tuku (lipogenezí). Stejná cesta přes aktivovanou PI-3-K vede k hypoglykemizujícímu efektu inzulínu. Glukózové transportéry (GLUT-4) závislé na inzulínu se přesunou z nitra buňky k jejímu povrchu, přičemž se otevřou transportní kanály pro glukózu a glukóza vstupuje do buňky. Tímto mechanismem se reguluje postprandiální glykémie ve tkáních závislých na účinku inzulínu (tj. ve svalové a tukové tkáni). V játrech se za fyziologických poměrů uskutečňuje facilitovaná difúze glukózy, která nevyžaduje inzulín. Druhá cesta z aktivovaného inzulínového receptoru vede přes mitogen aktivovanou proteinkinázu (MAP kinázu), která se projevuje změnami v expresi genů včetně proteoanabolického efektu inzulínu a zejména růstovými účinky.
Fyziologické působení inzulínu
Zmíněné děje, jejichž průběh je v podrobnostech mnohem složitější, jsou udržovány v rovnováze řadou zpětných vazeb, na nichž se podílejí vztahy mezi výší koncentrace glukózy v plazmě a inzulínem a současně se uplatňuje složitější rovnováha mezi inzulínem a kontrainzulárními hormony, včetně hormonů trávicí trubice. Nejde jen o vzájemné působení inzulínu, glukagonu, katecholaminů, růstového hormonu a kortizolu, ale regulace je ovlivněna i glukózo-dependentním inzulinotropním peptidem, uvolňovaným z K-buněk duodena (GIP, dříve označovaný jako žaludeční inhibiční peptid), nebo somatostatinem. Těmito hormony se uskutečňují regulace po stimulaci potravou, tedy v postprandiální fázi. Významné místo v regulaci sekrece i účinku inzulínu mají také volné mastné kyseliny.
Obr.: Závislost biologické odpovědi na koncentraci inzulínu
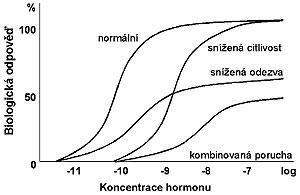
Je zřejmé, že fáze nalačno a fáze postprandiální se odlišují právě v zapojení jednotlivých regulačních mechanismů zprostředkovaných hormonálními i humorálními faktory. Pro pochopení vzniku a rozvoje inzulínové rezistence je třeba uvést alespoň základní poznatky o sekreci inzulínu. Po několika hodinách lačnění, kdy chybí stimulus vyvolaný potravou, se sekrece inzulínu ustaluje na nízkých hodnotách (tzv. bazální sekrece). Jedná se o sekreci pulsní(1), jejíž fyziologický význam zatím nebyl zcela jednoznačně objasněn, ale předpokládá se, že právě tento typ sekrece udržuje „citlivost“ (senzitivitu) cílových tkání k inzulínu. Při nízkých koncentracích inzulínu v plazmě (kolem 5-6 mU/l) je tak zachována dobrá vnímavost cílových buněk, a tím i jejich přiměřená odpověď.
Pulsní uvolnění inzulínu ze sekrečních granulí B-buněk v postprandiální fázi sekrece (časná fáze sekrece) způsobí přísun hormonu k cílové buňce, jejíž citlivost je vysoká a odezva poté mohutná. Je-li stimulus pro sekreci inzulínu větší nebo působí-li déle (např. vlivem jídla), přechází sekrece inzulínu po několika minutách do druhé fáze sekrece, během níž se syntetizují nové molekuly inzulínu (pozdní fáze sekrece). Příliv většího množství inzulínu k cílové buňce, který trvá déle, způsobí další reakce. Protrahovaná sekrece inzulínu by totiž vedla ke značnému poklesu glykémie v pozdním stadiu postprandiální sekrece, která by se mohla projevit těžkou hypoglykémií. Za fyziologické situace však k tomu nedochází, protože regulační mechanismy, uplatňující se jak v cílové buňce, tak v B-buňce, znemožní, aby došlo k nekontrolovanému účinku i sekreci inzulínu. V cílové buňce probíhá „regulace inzulínových receptorů dolů“ (tzv. down-regulation), která vzniká velmi rychle vlivem výrazného obsazování receptorů inzulínem. Receptory s navázaným inzulínem pak fúzují v membráně a vytvářejí shluky (tzv. clustery), které podnítí smrštění kontraktilních fibril uložených pod buněčnou membránou. Membrána s nahromaděnými receptory se pak začne vchlipovat do nitra buňky, vzniká nejdříve tzv. potažená jamka (coated pit), která se později na úrovni obvodu zaškrtí, přičemž vznikne tzv. potažený váček (coated vesicle). Tyto váčky uložené uvnitř buňky obsahují komplexy receptorů s navázaným inzulínem. Tím klesá počet inzulínových receptorů na membráně a zároveň klesá i schopnost buňky vázat inzulín (ovlivněním vazebných parametrů). Mechanismus této regulace receptorů dolů umožňuje, aby po nadměrném přívodu inzulínu nedošlo k fatální hypoglykémii. Děj probíhá velmi pružně a změnu vazebných charakteristik lze prokázat již po několika minutách. Při přechodu z postprandiálního stadia do lačnění či až hladovění se objevují pochody opačné, kdy může nastávat regulace receptorů „nahoru“ (tzv. up-regulation). Receptory recyklují, a tím rychle reagují na aktuální poměry podmíněné nadbytkem nebo nedostatkem inzulínu.
U jedinců s výbornou citlivostí na inzulín jsou uvedené děje velmi jemně regulovány. Zpětnou vazbou, vyvolanou jednak klesající koncentrací glukózy v plazmě a jednak hormonálně glukagonem a somatostatinem, se tlumí sekrece inzulínu. Obnovuje se rovnováha, takže glykémie neklesne pod dolní hranici normálních hodnot.
Rozvoj inzulínové rezistence
Jedinec, u něhož existují výše popsané vztahy a regulační mechanismy, má normální působení inzulínu. Jsou však stavy, které uvedené mechanismy narušují, a ty pak vedou ke sníženému účinku inzulínu - k inzulínové rezistenci. Jde o situaci, při níž fyziologické množství inzulínu vyvolá sníženou biologickou odpověď, takže k dosažení přiměřené reakce je zapotřebí většího množství hormonu. Cílová buňka tudíž reaguje subnormálně a výsledek její aktivity je nižší jak po stránce metabolických efektů, tak v transportu glukózy. Regulační zpětnovazebné mechanismy umožní v organismu nastolit novou rovnováhu, při níž zvýšené požadavky podmíní vyšší sekreci inzulínu z B-buňky, a ta udrží při jeho vyšší plazmatické hladině děje na přijatelné úrovni. Proto tento stav lze označit jako kompenzovaný. Zůstane zachován také transport glukózy do svalové a tukové buňky. Jedinec má normální glykémii a současně ještě normální toleranci glukózy. Tuto situaci běžně způsobuje přejídání. Zejména kombinace se sníženou fyzickou aktivitou pak vede ke vzrůstu tělesné hmotnosti. Děj je reverzibilní a úprava životosprávy s poklesem kalorického příjmu a zvýšením fyzické aktivity může zcela upravit původní inzulínovou senzitivitu.
Trvá-li zvýšená tělesná hmotnost déle, postupně se prohlubuje porucha citlivosti na inzulín, a navíc mohou selhat uvedené regulační mechanismy. To nastává u jedinců, kteří mají skrytou genetickou predispozici ke vzniku této poruchy. Nejprve vzniká zvýšená postprandiální hyperinzulinémie (jak co do výše, tak délky trvání zvýšené koncentrace inzulínu v plazmě), později i hyperinzulinémie bazální, neboť B-buňka se pro zvýšené nároky cílových tkání nevrací do zcela fyziologické bazální sekrece. Tím se soustavně narušuje vztah mezi hladinou inzulínu a cílovou buňkou a mezi efektem inzulínu a jeho potřebou v organismu.
Závislost efektu inzulínu na koncentraci hormonu lze vyjádřit graficky (Obr. 1). Snížení citlivosti (senzitivity) na inzulín podmiňuje posun této křivky doprava, takže požadovaného maximálního efektu lze dosáhnout při vyšší hladině inzulínu. Naopak při poruše v odezvě (anglicky tzv. responsiveness) ani vyšší dávka inzulínu nevede k dosažení maximální odpovědi. U mnoha stavů se jedná o kombinaci obou typů změn. Porucha může být lokalizována kdekoli na cestě mezi samotnou molekulou inzulínu a reakcemi uvnitř cílové buňky. Často se proto užívá při klasifikaci inzulínové rezistence rozlišení poruch na prereceptorové, receptorové a postreceptorové (Tab.). Změny jsou podmíněny jednak vlivy genetickými, jednak vlivy zevního prostředí. Již samotné abnormality molekuly inzulínu či proinzulínu mohou vést k jeho nižšímu účinku, a tím i ke snížené odpovědi, která se nezlepší ani při vyšší koncentraci hormonu. Také přítomnost protilátek proti inzulínu značně oslabuje jeho účinek, který má charakter snížené senzitivity. Blokáda sekrece inzulínu hormonální povahy (např. somatostatinem) se promítá do prereceptorové úrovně, jindy se efekt hormonu rozvine v důsledku ovlivnění postreceptorových dějů (steroidy, které ovlivní i sekreci inzulínu). Na výsledném stavu se velmi často podílejí kombinace uvedených změn, kdežto izolované postižení pouze jedné z nich bývá spíše vzácné.
Inzulínová rezistence způsobená abnormalitou receptoru (např. při patologické primární struktuře receptoru s postižením vazebného místa pro inzulín) je extrémně vzácná. Také protilátky proti inzulínovému receptoru se vyskytují zcela výjimečně. Vedle blokujících protilátek, které vedou ke sníženému účinku inzulínu, byly prokázány též stimulující protilátky, které aktivují receptor, a tím vyvolají hypoglykémii. Vazba takové protilátky působí synergicky s inzulínem a zvyšuje tudíž odpověď. K regulaci inzulínových receptorů dolů s poklesem vazby inzulínu dochází akutně vlivem prandiální sekrece inzulínu, kdežto při chronické hyperinzulinémii se uplatňuje mnohem méně, než se dříve myslelo.
Při rozvoji inzulínové rezistence se nejvíce uplatňují změny postihující postreceptorové děje. Sem patří jak uvedený model sníženého působení inzulínu při narůstající hmotnosti (obezita), tak metabolický syndrom a též diabetes mellitus 2. typu. Stavy s inzulínovou rezistencí se značně liší podle přítomnosti genetické vlohy, která podstatně znesnadňuje její ovlivnění na rozdíl od prostého přejídání a snížené fyzické aktivity, které obecně zhoršují působení inzulínu. V případě genetické podmíněnosti se uvažuje v patogenezi inzulínové rezistence o tzv. kandidátních genech, jako je tomu např. u metabolického syndromu. Dosavadní poznatky nasvědčují, že se nejedná o postižení jednoho genu, ale že inzulínová rezistence je následkem mozaiky polygenně se vyskytujících polymorfismů. Genetická podmíněnost může být významná zejména v rámci diabetu 2. typu, kdežto v případě obezity bývá její podíl různý. Podíl exogenních a endogenních příčin v patogenezi inzulínové rezistence může ovlivňovat jak účinnost léčebných opatření, tak i prognózu jedince.
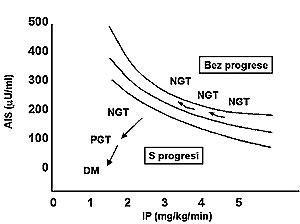
Obr.:Vztah časné sekrece inzulínu (AIS) k působení inzulínu (IP). Osoby s normální tolerancí glukózy (NGT), porušenou tolerancí (PGT a diabetem (DM)
Ve skupině postreceptorových poruch vyvolávajících inzulínovou rezistenci se využívá modelových pokusů s kmeny myší, u nichž chybí např. gen pro IRS-1 nebo IRS-2 (tzv. knockout geny). Chybění genu pro IRS-1 vede u myši k výrazné periferní rezistenci na inzulín a současně k vystupňované sekreci inzulínu z B-buňky, která udrží toleranci glukózy (myš nedostane diabetes). Naopak v případě chybění IRS-2 porucha působení inzulínu (inzulínová rezistence) je provázena poruchou jeho sekrece a u myši se manifestuje diabetes 2. typu. Tento model zároveň demonstruje propojenost obou úrovní, tj. sekrece a působení inzulínu při rozvoji diabetu 2. typu(2). Zda se podobný mechanismus může podílet také na rozvoji lidského diabetu 2. typu, dosavadní výsledky zatím neprokázaly.
Sekrece a působení inzulínu
Mezi sekrecí inzulínu a jeho periferním působením existuje hyperbolický, tedy inverzní vztah (Obr. 2)(3). U jedinců s vysokou citlivostí na inzulín je přítomna nízká sekrece inzulínu, kdežto nárůst rezistence je provázen vyšší sekrecí inzulínu. Tyto vztahy je možno prokázat ze spotřeby glukózy infundované při hyperinzulinemickém euglykemickém clampu, tj. stavu ustálené glykémie. Zatímco v prvním případě je spotřeba glukózy vysoká, při rezistenci se množství infundované glukózy snižuje. U každého jedince může být hyperbolická závislost umístěna v jiné vzdálenosti od průsečíku os, což může být i geneticky podmíněno vedle efektu hmotnostního indexu BMI. S nárůstem BMI se hyperbola vzdaluje od průsečíku os, neboť se současně snižuje inzulínová senzitivita. Posun z hyperbolické křivky směrem k průsečíku os znamená kvalitativní změnu v toleranci glukózy a jedinci jsou pak označeni jako osoby s progresí, jak je patrno z Obr. 2.
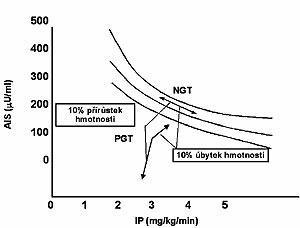
Ne u každého jedince s inzulínovou rezistencí podmíněnou hmotnostním přírůstkem se musí vyvinout diabetes. Při zachované dostatečné sekreční kapacitě slinivky se podaří někdy i velmi vystupňovaným výdejem inzulínu udržet normální toleranci glukózy při výrazné inzulínové rezistenci (dojde pouze k posunu na dané hyperbole). U takového jedince se nepředpokládá genetická dispozice k diabetu. Jindy i malá porucha v působení inzulínu vede k manifestnímu diabetu 2. typu, což podporuje představu o genetické podmíněnosti. Vliv změny hmotnosti na sekreci a působení inzulínu je patrný z Obr. 3. Při normální glukózové toleranci dochází k posunu po hyperbole, takže např. hmotnostní úbytek je spjat se zvýšenou senzitivitou na inzulín a současně se sníženou sekrecí hormonu(4). Naopak u porušené glukózové tolerance a podobně i u diabetu znamená obdobný hmotnostní přírůstek při relativně malém snížení inzulínové senzitivity zřetelnou změnu sekrece, jejíž pokles vyjadřuje neschopnost slinivky kompenzovat nárůst inzulínové rezistence. Následkem je pak zhoršená tolerance glukózy při relativní nebo absolutní hypoinzulinémii.
Sekrece a působení inzulínu jsou vzájemně propojeny, jak vyplývá z uvedeného schématu, ale zatím nebyla objasněna patogeneze tohoto vztahu.
Obr.: Vliv úbytku a přírůstku hmotnosti na vztahy mezi sekrecí inzulínu (AIS) a působením inzulínu (IP) u osob s normální (NGT) a porušenou (PGT) glukózovou tolerancí
Vztah inzulínové rezistence k metabolickým změnám
Inzulínová rezistence se projevuje jednak v játrech, jednak v tukové nebo svalové tkáni. Relativní nedostatek inzulínu při inzulínové rezistenci vede k neschopnosti potlačit glukoneogenezi v játrech. Vytváří se více glukózy, na jejímž odsunu z cirkulace pak závisí stupeň glykoregulační poruchy. Nepotlačí-li příslušná hladina inzulínu glukoneogenezi v játrech při současně snížené citlivosti na inzulín ve svalové a tukové tkáni, objevuje se hyperglykémie nalačno, jako je tomu typicky při diabetu 2. typu. Výše glykémie pak bývá výrazem stupně rezistence. Zlepšený účinek inzulínu např. vlivem hmotnostního úbytku či vyšší fyzické aktivity je provázen poklesem glykémie nalačno.
Na rozvoji inzulínové rezistence se významně podílejí i lipidy a v současné době se považují dokonce za základní příčinu jejího vzniku. Fyziologicky působí volné mastné kyseliny jako významný stimulátor sekrece inzulínu, a to synergicky s glukózou(5). Při poklesu hladiny mastných kyselin v průběhu hladovění klesá i stimulační efekt glukózy na B-buňky, takže sekrece inzulínu klesá. Bylo prokázáno, že inzulinotropní efekt mastných kyselin stoupá s délkou řetězce a se stupněm jejich nasycení(6). Z toho vyplývá, že intenzita sekrece inzulínu nezávisí jen na koncentraci glukózy, ale též na koncentraci a typu cirkulujících mastných kyselin. Citlivost B-buňky, a tedy i sekreční odpověď jsou závislé nejen na oscilaci hladin glukózy, ale i mastných kyselin. Krátkodobě působí volné mastné kyseliny stimulaci sekrece inzulínu. Při dlouhotrvajícím zvýšení hladin mastných kyselin je sekreční stimul natolik výrazný, že se dostavuje hyperinzulinémie, a to dokonce vyšší, než by odpovídalo hladině glukózy. Současně se tlumí sekrece inzulínu stimulovaná glukózou a snižuje se exprese genu pro inzulín(7). Postupně tak dochází naopak k negativnímu účinku chronicky zvýšené hladiny volných mastných kyselin na sekreci inzulínu a k následné hypoinzulinémii.
Vyšší přísun volných mastných kyselin do svalové tkáně podmiňuje pokles utilizace glukózy, neboť se předpokládá podle koncepce Randlova cyklu snížení oxidace glukózy vlivem zvýšené oxidace mastných kyselin(8). V principu jde o snížení glykolýzy ve svalu při inhibici fosfofruktokinázy následkem zvýšené koncentrace citrátu. Zároveň je inhibována pyruvát dehydrogenáza zvýšenou koncentrací acetylkoenzymu A.
Počáteční hyperinzulinémie se kombinuje s inzulínovou rezistencí, která se zvýrazňuje ukládáním lipidů (především triacylglycerolů) ve svalové tkáni, játrech a v B-buňce. Volné mastné kyseliny, uvolněné zejména z viscerální tukové tkáně (jejich zdrojem může být i potrava při zvýšené konzumaci), totiž vstupují do B-buňky (podobně dochází k infiltraci v játrech a svalu), kde nejsou oxidovány v mitochondriích beta-oxidací, neboť je blokován jejich transportní enzym karnitinpalmityltransferáza (CPT-1) malonylkoenzymem A. Tato látka svým inhibičním efektem na CPT-1 způsobí, že aktivní forma volných mastných kyselin (acylkoenzym A) se naopak využije k syntéze triacylglycerolů, jejichž zvýšené množství uvnitř buňky spolu s diacylglycerolem (DAG) jako meziproduktem pak tlumí metabolismus glukózy a prohloubí inzulínovou rezistenci(9). Molekula DAG stimuluje aktivity proteinkináz C (PKC), které fosforylují serin a threonin v molekulách proteinů regulujících přenos signálu uvnitř buňky (např. IRS), a tím dochází ke snížení efektu inzulínu. Jedním z prvních negativně ovlivněných pochodů ve svalové tkáni je transport glukózy řízený transportéry GLUT4. Příčinou je abnormální fosforylace IRS a fosfatidyl-inositol-3-kinázy, které přímo regulují přemístění transportérů GLUT4 k buněčné membráně(10). Již samotná dietní opatření omezující přívod tuků vedou ke snížení obsahu lipidů v myofibrilách a současně zlepší účinek inzulínu projevující se vzestupem exprese transportéru GLUT4(11). Popsaný děj souvisí s aktivitou PKC, takže použití inhibitoru PKC zlepšuje účinek inzulínu ovlivněním kaskády fosforylačně-defosforylačních reakcí.
Úloha lipotoxicity při selhání B-buňky
Primárně inzulinotropní působení volných mastných kyselin na B-buňku chrání organismus před ketózou při jejich nadměrném akutním uvolnění z tukové tkáně. Přetrvávající zvýšený přísun volných mastných kyselin však vede k infiltraci B-buněk triacylglyceroly, a tím k jejich postupnému selhávání, k útlumu sekrece i syntézy inzulínu. Dochází pak hypoinzulinémii, která prohlubuje změny způsobené inzulínovou rezistencí v periferních tkáních. Tento dlouhodobý nežádoucí účinek zejména volných mastných kyselin a triacylglycerolů je označován pojmem lipotoxicita(12). V Langerhansových ostrůvcích byla popsána zvýšená apoptóza(13). Z posloupnosti popsaných změn pak vyplývá nejen možnost rozvoje diabetu 2. typu, ale i postupné zhoršování již existujícího diabetu(14). Je totiž zřejmé, že hyperglykémie se může vlivem porušeného lipidového metabolismu dále zhoršovat, takže pak přistupuje i chronický efekt zvýšené koncentrace glukózy, tj. glukotoxicita. Oba efekty (lipotoxicita a glukotoxicita) tudíž negativně ovlivňují sekreci inzulínu, která po počáteční fázi trvalého zvýšení se obrací a postupně se snižuje až do hypoinzulinémie. Dlouhodobá expozice zvýšené hladině mastných kyselin má tedy na sekreci inzulínu opačný efekt než krátkodobý vzestup.
Diabetes lipidus, či mellitus?
Novější poznatky o metabolismu při inzulínové rezistenci ukazují, že metabolismus lipidů a sacharidů je ve velmi těsném vztahu. Současně je zřejmé, že krátkodobý vzestup jak glykémie, tak hladiny volných mastných kyselin má zcela protichůdný efekt na sekreci inzulínu i na jeho působení v cílové tkáni než dlouhodobý efekt zvýšených koncentrací. Stimulační účinek mastných kyselin podmiňující nejprve hyperinzulinémii a inzulínovou rezistenci se s dobou expozice mění. Inzulínová rezistence, na níž se podílí metabolismus mastných kyselin a infiltrace cílových tkání, především svalové tkáně a jater triacylglyceroly, je provázena jak hyperinzulinémií, tak později hypoinzulinémií. Právě účinkem lipidů je propojena sekrece inzulínu s jeho působením. Úloha mastných kyselin a poruchy metabolismu lipidů se považují v patogenezi inzulínové rezistence, ale též v patogenezi diabetu 2. typu za zásadní a někteří autoři je hodnotí jako primární. Proto nepřekvapí označení jako diabetes mellipidus nebo diabetes lipidus či lipomellitus(15). Z tohoto pohledu se můžeme orientovat při chápání diabetu 2. typu a inzulínové rezistence spíše lipocentricky než glukocentricky.
Literatura
1. WALLUM, BJ., KAHN, SE., McCULLOCH, DK., PORTE, D. Insulin secretion in the normal and diabetic human. In ALBERTI, KGMM., et al. International Textbook of Diabetes mellitus. J. Wiley & Sons Ltd., 1992, p. 285-302.
2. AGUIRRE, V., WHITE, MF. Dysregulation of IRS-proteins causes insulin resistance and diabetes.Curr Opin Endocrinol Diab, 2000, 7, p. 1-7.
3. WEYER, C., BOGARDUS, C., MOTT, DM., et al. The natural history of insulin secretory dysfunction and insulin resistance in the pathogenesis of type 2 diabetes mellitus.J Clin Invest, 1999, 104, p. 787-794.
4. WEYER, C., HANSON, K., BOGARDUS, C., et al. Long-term changes in insulin sensitivity and insulin secretion associated with gain, loss, regain and maintenance of body weight. Diabetologia, 2000, 43, p. 36-46.
5. BODEN, G., CHEN, X., IQBAL, N. Acute lowering of plasma fatty acids lowers basal insulin secretion in diabetic and non-diabetic subjects.Diabetes, 1998, 47, p. 1609-1612.
6. STEIN, DT., STEVENSON, BE., CHESTER,MW., et al. The insulinotropic potency of fatty acids is profoundly influenced by their chain length and degree of saturation.J Clin Incest, 1997, 100, p. 398-403.
7. JACQUEMINET, S., BRIAUD, I., ROUAULT, C., et al. Inhibition of insulin gene expression by long-term exposure of pancreatic beta-cells to palmitate is dependent upon the presence of a stimulatory glucose concentration. Metabolism, 2000, 49, p. 532-536.
8. RANDLE, PJ., GARLAND, PB., HALES, CN., et al. The glucose fatty-acid cycle: Its role in insulin sensitivity and the metabolic disturbances of diabetes mellitus.Lancet, 1963, 1, p. 785-789.
9. PAN, DA., LILLIOJA, S., KRIKETOS, AD., et al. Skeletal muscle triglyceride concentrations are inversely related to insulin action. Diabetes, 1997, 46, p. 983-988.
10. DRESNER, A., LAURENT, D., MARCUCCI, M., et al. Effects of free fatty acids on glucose transport and IRS-1-associated phosphatidylinositol-3-kinase activity. J Clin Incest, 1999, 103, p. 253-259.
11. GRECO, AV., MINGRONE, G., GIANCATERINI, A., et al. Insulin resistance in morbid obesity. Reversal with intramyocellular fat depletion. Diabetes, 2002, 51, p. 144-151.
12. McGARRY, JD., DOBBINS, RL. Fatty acids, lipotoxicity and insulin secretion. Diabetologia, 1999, 42, p. 128-138.
13. LUPI, R., DOTTA, F., MARSELLI, L., et al. Prolonged exposure to free fatty acids has cytostatic and pro-apoptotic effects on human pancreatic islets. Diabetes, 2002, 51, p. 1437-1442.
14. McGARRY, JD. Dysregulation of fatty acid metabolism in the etiology of type 2 diabetes. Diabetes, 2002, 51, p. 7-18.
15. SHAFRIR, E., RAZ, I. Diabetes: mellitus or lipidus? Diabetologia, 2003, 6, p. 433-440
Prof. MUDr. Jan Škrha, DrSc.
Univerzita Karlova v Praze, 1. LF a VFN, III. interní klinika endokrinologie a metabolismu
e-mail: jan.skrha@lf1.cuni.cz
