V postgraduálně zaměřeném časopise rozdělujeme komplexní faktory důležité pro volbu optimální antiepileptické léčby z hlediska didaktického a názorného do dvou základních skupin, respektive na dvě osy: osa I zohledňuje klasický výběr léčby podle typu epileptických záchvatů/syndromu a navíc podle širších priorit konkrétního léku. Osa II zohledňuje volbu léčby podle konkrétního typu, individuality pacienta v jeho plné šíři, zejména podle jeho somatické a psychické kondice.
Summary
Hovorka, J. Choice of optimal antiepileptic treatment on two axes: Axis I. according to the type of epileptic seizure/syndrome and the priorities of antiepileptics; axis II. According to patient's type, individuality
Current options of pharmacological treatment of epilepsy are very broad. They allow us to go further than just to the schematic treatment option depending on the type of epileptic seizure/syndrome. In our article we divide the complex factors important for choosing the optimal antiepileptic treatment on two axes: Axis I reflects the classic choice of treatment depending on the type of epileptic seizure/syndrome and also by the wider priorities of a particular drug. Axis II. reflects the choice of treatment according to a specific patient's type, individuality in its full breadth, and especially according to the patient's somatic and mental condition.
Naše sdělení navazuje na systematicky zpracovávané téma týkající se epilepsie a její léčby v tomto časopise, zejména pak v šestém čísle z roku 2005. Zde byly mimo jiné uceleně zpracovány zásady farmakoterapie u epilepsie.(1) Tyto údaje jsou pro čtenáře internetově dobře dostupné (www.postgradmed.cz) a z hlediska taktiky a volby léčby jsou nadále platné. Problematika léčby epilepsie je v naší, dobře dostupné literatuře průběžně aktualizována.(2–8) V práci se zaměřujeme na současné široké možnosti individuální volby antiepileptické léčby. Je to umožněno narůstající nabídkou dnes dostupných antiepileptik. Volba konkrétní antiepileptické léčby je závažným rozhodnutím. Většina pacientů jí bude užívat řadu let, ne-li celoživotně, a to v různých životních etapách.
V tomto kroku je proto nutno zohlednit více než jen volbu antiepileptika podle spektra jeho účinnosti. Přehled řady faktorů ovlivňujících volbu antiepileptické léčby uvádíme v Tab. 1.(9)
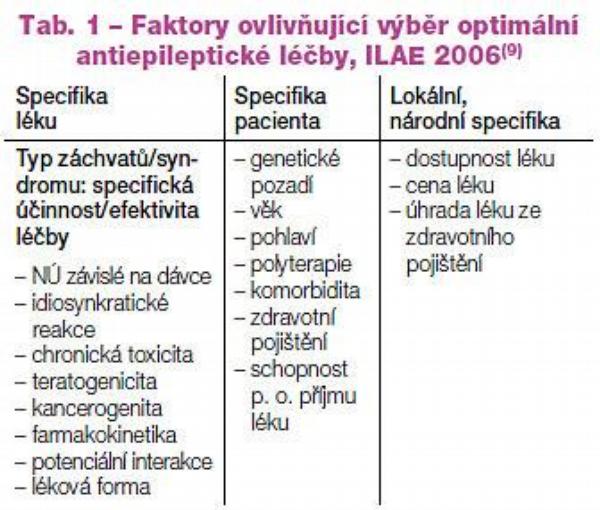
V postgraduálně zaměřeném časopise rozdělujeme tyto komplexní faktory z didaktického hlediska do dvou základních skupin, respektive na dvě osy: osa I zohledňuje klasický výběr léčby podle typu epileptických záchvatů/syndromu a navíc podle širších priorit konkrétního léku. Osa II zohledňuje volbu léčby podle konkrétního typu, individuality pacienta v jeho plné šíři, zejména podle jeho somatické a psychické kondice. Věříme, že toto didaktické členění může být užitečným vodítkem pro optimální volbu většinou dlouhodobé antiepileptické léčby v klinické praxi.
Volba antiepileptické léčby na ose I: podle typu epileptických záchvatů/syndromu a podle priorit léku
Taktika léčby: zásady iniciální, případně alternativní monoterapie a racionální polyterapie zůstávají stejné.
Kdykoli je to možné, pacienti s nově diagnostikovanou epilepsií mají být iniciálně léčeni monoterapií. V případě neúspěchu je doporučována alternativní monoterapie, obvykle alespoň dalším jedním či dvěma léky.(1, 2, 10–13) Přehodnocení neúspěšnosti monoterapie vždy předchází rozhodnutí o polyterapii. Jde především o vyloučení „pseudofarmakorezistence“. Problematika pseudofarmakorezistence je dostupná v naší literatuře a odkazujeme na ni.(14) Je nutno zodpovědět následující otázky: Trpí nemocný skutečně epilepsií, nejde o jiné neepileptické záchvaty somatické či psychogenní či jejich koincidenci? Byla správná syndromologická diagnóza epilepsie a odpovídá tomu volba antiepileptik? Byly dávky léků v monoterapii dostatečné a při neúčinnosti vytitrované do maximálních tolerovaných dávek? Byla dobrá compliance nemocného při užívání léků, je pacient k léčbě motivován, nezapomíná na pravidelnou léčbu? Byla dobrá compliance nemocného v režimové léčbě, zvláště u některých syndromů, kde jsou provokační faktory významné?
Pokud není monoterapie dostatečně úspěšná, přistupujeme k tzv. „racionální polyterapii“. Pojem „racionální polyterapie“ je definován spíše svým opakem: měl by zdůraznit to, že polyterapie není „iracionální“, chaotická, indikovaná na základě špatné syndromologické diagnózy, nevhodné volby léků, jejich kombinací a dávek.(13) Za prospěšnou se dnes požaduje kombinace maximálně dvou až tří antiepileptik.
Polyterapie, respektive přídatná léčba, má své výhody a nevýhody.(11, 13) V řadě případů ji není nutno zbytečně odkládat, může být účinnější i lépe tolerovaná. V případě farmakorezistence, kdy pacient nereaguje dostatečně na adekvátní léčbu, by mělo být včas, do jednoho až dvou let, indikováno vyšetření ve specializovaném centru. Včas by měla být zvážena léčba invazívní (klasická epileptochirurgická, stimulační, event. nověji radiofrekvenční – koagulační).(6, 8, 15)
Volba léku podle typu epileptického záchvatu/syndromu
Základním a tradičním vodítkem pro volbu antiepileptika je typ záchvatu/syndromu, tedy faktory „seizure/syndrome related“, a to v monoterapii i v kombinované léčbě.
Konkrétní vodítka jsou dobře známá, internetově dostupná. V ČR byla vypracována skupinou EpiStop,(1, 2) v širší verzi jsou pak často citována doporučení NICE.(16) (Tab. 2, 3)
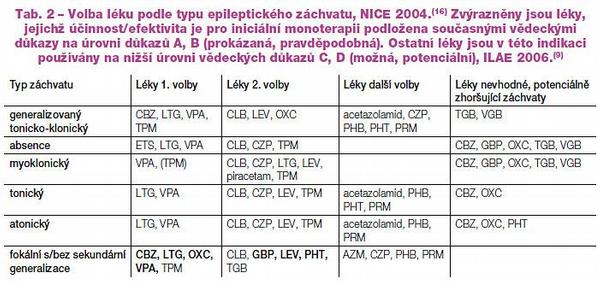
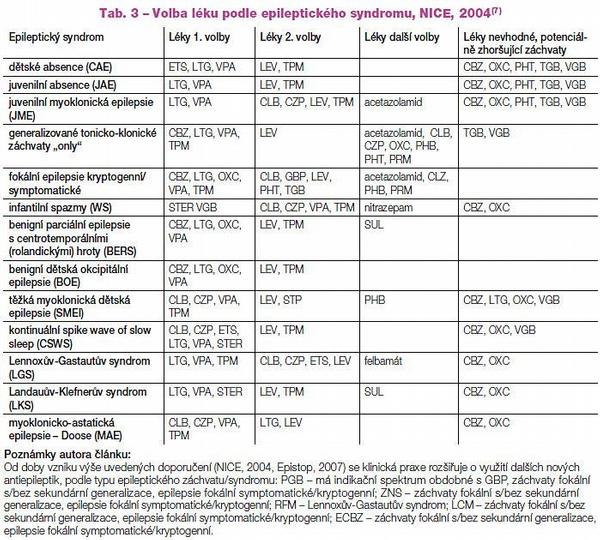
Je zajímavé, jak málo jsou současně užívaná vodítka pro volbu léčby podložena vědeckými důkazy na nejvyšší úrovni důkazů A, B (účinnost prokázaná, pravděpodobná).(7, 9) Uvádíme to na příkladu iniciální monoterapie v Tab. 2.(8, 9) Užití léků, které je v této indikaci podloženo vědeckými důkazy na úrovni A, B, je v tabulce zvýrazněno. V klinické praxi je tak volba ostatních léků podložena nižší úrovní vědeckých důkazů C, D (účinnost možná, potenciální).(9) Některá antiepileptika mohou paradoxně určité typy záchvatů agravovat, například: GTCS (záchvaty generalizovaných tonicko-klonických křečí) – TGB, VGB, absence, myoklonické záchvaty – CBZ, GBP, OXC, TGB, VGB. Údaje o agravaci záchvatů nejsou, až na jednu výjimku, v české verzi EpiStop(2) uvedeny. Byly však u nás publikovány formou přehledného článku(17) a jsou dostupné v tabelárním přehledu NICE guidelines (Tab. 2).(16)
Zjednodušeně řečeno, širokospektrá antiepileptika (VPA, LTG, TPM, LEV, ZNS) agravaci záchvatů nevyvolávají. Můžeme je tedy využít tam, kde si konkrétním typem záchvatů či syndromu nejsme jisti, případně tam, kde se u pacienta vyskytuje více typů záchvatů. Širokospektrá antiepileptika jsou některými autory považována za optimální pro přídatnou, kombinovanou léčbu.
Naopak antiepileptika s užším spektrem účinku (např. u fokální epilepsie – CBZ, OXC, GBP, PGB, TGB, VGB, u absencí – ETS) jsou účinná jen u některých typů záchvatů. Většinou tedy jde o léky indikované u fokálních epilepsií, naopak zhoršující idiopatické generalizované epilepsie. Na tyto aspekty je při volbě antiepileptické léčby podle osy I – „seizure related“ – nutno vždy myslet. Shrnujeme je uceleně v Tab. 4.
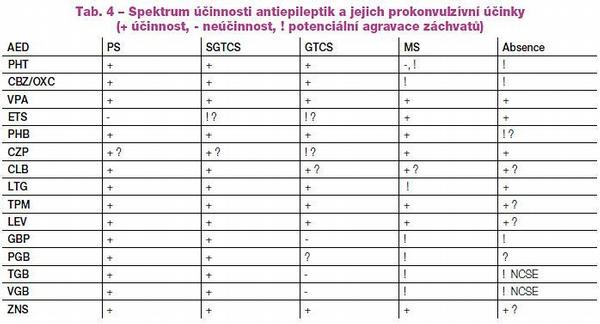
I přes relativně dlouhodobější znalost uvedené problematiky se její uplatnění v klinické praxi prosazuje v širší míře až v posledních letech. Nevhodně volená léčba podle typu záchvatu/syndromu není dosud zdaleka vzácným příkladem „fseudofarmakorezistence“. Řešení je obvykle elegantní a radostné: stačí změnit antiepileptikum s užším spektrem účinku za širokospektré.
Volba antiepileptika podle jeho priorit
Volba antiepileptika podle spektra účinnosti na typ záchvatů/syndromu, event. podle potenciální agravace záchvatů představuje první a základní krok při rozhodování o léčbě. Více faktorů však nezohledňují. Nástup nových, moderních a různorodých antiepileptik umožnil širší pohled na volbu léčby. Jde o řadu dalších vlastností, „treatment-related“ faktorů, která antiepileptika mají.
Vedle spektra účinnosti zahrnují i jeho sílu, mechanismy účinku, tolerabilitu, rychlost titrace, interakce přidávaného antiepileptika s ostatními antiepileptiky a léky, rozsah monitorování léčby aj.(18) V Tab. 5 uvádíme základních šest priorit na příkladu nových antiepileptik.(13,18–20)
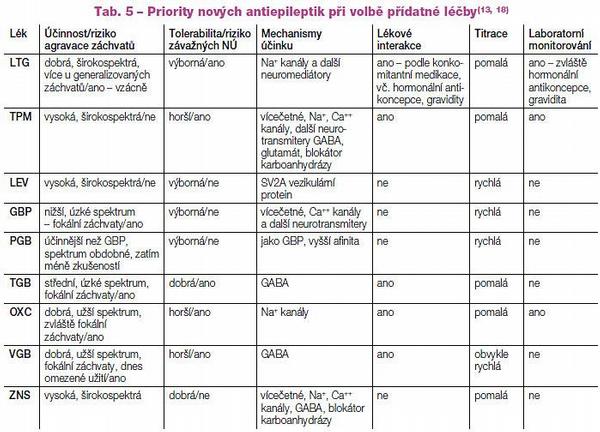
Podle klinické potřeby můžeme individuálně volit lék silnější/slabší, tolerovaný obvykle výborně/hůře, s možností rychlé titrace/s nutností pomalé titrace (Tab. 6), bez lékových interakcí/s lékovými interakcemi (antiepileptika, ostatní léky) (Tab. 7), bez nutnosti laboratorní monitorace/s laboratorní monitorací (hladiny léku, biochemie, krevní obraz) a také můžeme volit léky s různými mechanismy účinku v alternativní monoterapii i v kombinované léčbě (Tab. 8).
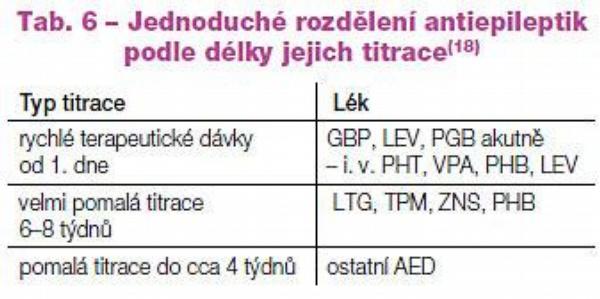
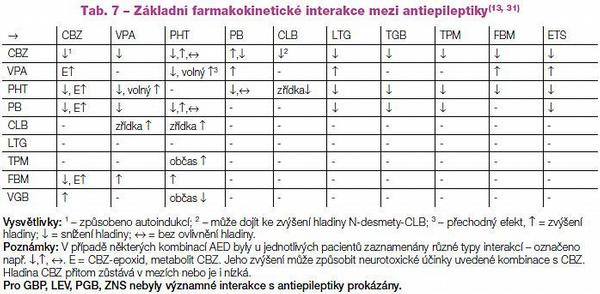
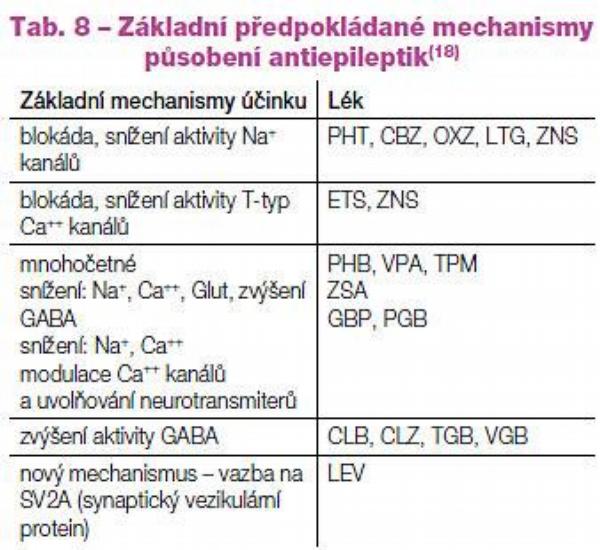
Například při nutnosti rychlé titrace musíme volit lék s adekvátním titračním schématem, byť např. na přechodnou dobu. Naopak rychlou, až překotnou titrací léku s nutností pomalé titrace můžeme pacienta osudově připravit o lék, na kterém mohl být plně kompenzovaný.
Z hlediska uvedených priorit je v posledních letech věnována pozornost možnostem volby antiepileptické léčby podle mechanismů účinku (Tab. 8). Souvisí to se zmíněným nástupem nových antiepileptik. Základní předpoklad tohoto přístupu je obdobný pro monoterapii i kombinovanou léčbu. Pokud budeme volit lék „pouze“ podle typu záchvatu/syndromu, můžeme v alternativní monoterapii i v kombinované léčbě užívat sice různé léky registrované k tomuto použití, nicméně mnohdy s obdobnými mechanismy účinku. Lze očekávat, že tento postup nemusí být příliš úspěšný.
Pokud naopak v alternativní monoterapii či v kombinované léčbě podáme léky s různými mechanismy účinku, lze očekávat úspěšnost vyšší. V tomto ohledu se experimentální a některé klinické údaje týkají vlastně jen léčby. V případě kombinované antiepileptické léčby vznikají mezi léky farmakodynamické interakce, které lze zjednodušeně rozdělit do čtyř základních skupin: mohou být supraaditivní (synergické), aditivní, infraaditivní (antagonistické) nebo indiferentní. Týká se to účinků terapeutických i nežádoucích. Cílem kombinace je pochopitelně maximální posílení účinnosti (supraaditivní, aditivní efekt) s minimálním nárůstem nežádoucích účinků (infraaditivní, indiferentní). Některé příklakombinované dy experimentálně nalezených farmakodynamických interakcí, které podporují smysluplnost volby antiepileptické léčby podle mechanismu účinku, uvádíme v Tab. 9. Z tabulky je patrné, že kombinace antiepileptik s odlišnými mechanismy působení byly v experimentech účinnější.
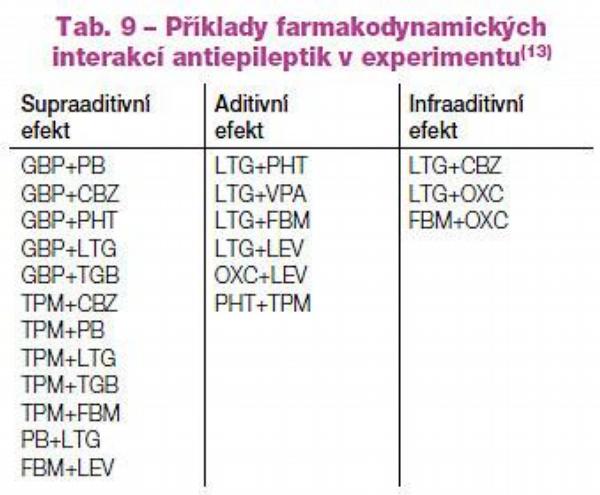
Klinických dat je méně.(13) Například u starších antiepileptik kombinace PHT a PB byla terapeuticky aditivní, z hlediska neurotoxicity infraaditivní. Obdobný byl výsledek studie VPA s CBZ nebo PB, avšak s aditivním efektem na neurotoxicitu.(21) Klinicky významný je aditivní účinek VPA s ETS(22) u absencí, s neurotoxicitou nižší, než byla pozorována při předchozí monoterapii VPA, respektive ETS. Snad nejcitovanější je studie potvrzující signifikantně významnější účinnost kombinace LTG a VPA, synergismus u léků s různými mechanismy účinku, oproti kombinacím LTG s CBZ či PHT u záchvatů parciálních i generalizovaných.(23)
I v současné době platí, že volba alternativní monoterapie a kombinované léčby je v klinické praxi založena spíše na publikovaných malých souborech pacientů, kazuistikách a na klinické empirii. Nicméně využití předpokládaných mechanismů účinku při volbě léčby má svoji logiku a může být v praxi přínosné. Odpovídají tomu i v současné době využívané kombinace antiepileptik: např. u fokální epilepsie CBZ + (VPA, LEV, GBP, PGB, TPM, ZNS aj.), LTG + (VPA, LEV, TPM, PGB, ZNS, VGB aj.) aj. kombinace, u generalizovaných idiopatických epilepsií např. VPA + (LTG, LEV, TPM, CZP aj.), LTG + (LEV, TPM, ETS, CZP aj.) aj.(1, 11, 13, 20)
Volba antiepileptické léčby na ose II: podle konkrétního typu, individuality pacienta
Zohlednění individuality pacienta je dalším základním vodítkem pro celostní pohled na léčbu nemocných s epilepsií. Antiepileptika totiž neovlivňují pouze průběh epilepsie, ale řadu dalších mozkových i tělesných funkcí a orgánů, u naprosté většiny nemocných na řadu let, ne-li doživotně. Ovlivňují tak celkovou, tělesnou a psychickou kondici nemocných s epilepsií, tedy jejich „funkční stav“. Právě dobrý funkční stav nemocných, optimální kvalita jejich života, jsou jediným a konečným cílem antiepileptické léčby. Zde se jedná o více než pouhou kompenzaci epileptických záchvatů.
Volba léčby podle typu pacienta – „patient related“ představuje velmi široký, relativně novější a mezioborový pohled na tuto problematiku.
Při volbě léčby tedy zohledňujeme konkrétní typ, individualitu pacienta v plné šíři: jeho věk, pohlaví, životní etapu (potenciálně fertilní ženy), tělesný a psychický stav, ostatní farmakoterapii, lékové interakce, ale i faktory psychosociální, ekonomické aj. Tento individuální výběr antiepileptické léčby umožnilo opět až rozšíření škály léků příchodem nových moderních antiepileptik. Zde uvádíme základní příklady některých častějších problémů dopadu antiepileptické léčby na celkový, interiktální stav nemocných. V dalších podrobnostech odkazujeme na dostupnou literaturu.
U dětí je například nutno zohlednit častější výskyt závažných hypersenzitivních reakcí na lék (rash u LTG, CBZ), hepatotoxických reakcí (VPA), kognitivního narušení (PHB, CBZ, TPM aj.), poruch chování (PHM BZD, LEV aj.), hypohidrózy a metabolické acidózy (acetazolamid, SUL, TPM, ZNS) aj.
Velmi široká a již tradiční je problematika léčby žen s epilepsií: kosmetické problémy (PHT, VPA), nadváha (VPA, VGB, GBP, PGB, CBZ), dospívání a hormonální funkce, poruchy reprodukce a metabolické poruchy u syndromu polycystických ovarií (VPA), interakce s kontraceptivy (induktory hepatálních enzymů CBZ, OXC, PHT, PHB, PRM snižují jejich spolehlivost, hormonální kontracepce naopak může ovlivnit plazmatickou koncentraci léků, např. LTG), riziko teratogenicity (polyterapie, vyšší dávky léků, zejména VPA), péče prekoncepční, plánování gravidity včetně optimalizace léčby, péče během gravidity (pravidelné kontroly pacientek – klinické, EEG, plazmatické hladiny léků, zohlednění nárůstu hmotnosti a dalších fyziologických změn v dávkování léků aj.), péče porodní, poporodní, kojení a nakonec problematika menopauzy.(1, 24–26)
Ovlivnění hormonálních funkcí zejména induktory hepatálních enzymů může být významné i u mužů.(1) Novějším tématem je léčba epilepsie u starších pacientů. Toto téma se však široce dotýká medicíny obecně,(27–32) klíčovými body jsou: – změna farmakodynamiky i farmakokinetiky ve vyšším věku (vyšší farmakosenzitivita, nižší dávky léků, možnost podávání léků i ve dvoudenních dávkách, např. u GBP); – lékové interakce s enzymatickými induktory (nejrizikovější je interakce warfarinu s induktory: při titraci nižší INR a jeho účinnost, při vynechání induktorů např. u noncompliance riziko krvácení, interakce s antihypertenzívy, hypolipidemiky, antidiabetiky, analgetiky, psychofarmaky aj.), významné lékové interakce naopak nevykazují GBP, PGB, LEV, ZNS, LTG; – častější výskyt neurotoxických nežádoucích účinků (útlum, kognice, závrativost, neobratnost, pády, zlomeniny, ovlivnění mobility); – častější hyponatrémie (CBZ, OXC); – výskyt osteopatií a až pětkrát častější výskyt zlomenin femuru a páteře u pacientů léčených enzymatickými induktory (změna léčby, event. suplementace Ca++, vitamínem D3, antiresorbční léčba aj.); – výběr a dávkování léků podle jejich eliminace a stavu orgánových funkcí (především renální eliminace – GBP, PGB, LEV, VGB, hepatální eliminace – ostatní antiepileptika); – častější výskyt úzkostných poruch a deprese aj., citlivé zohlednění volby antiepileptik dle jejich psychotropních účinků.
Nedoceněným tématem je problematika nadváhy, obezity ve vztahu k dlouhodobé antiepileptické léčbě. Jde o závažný rizikový faktor pro rozvoj dalších prognosticky významných zdravotních poruch, který se týká pacientů s epilepsií, tak jako ostatní populace. Zdaleka nejde jen o pacienty starší. Antiepileptika ovlivňují různou měrou tělesnou hmotnost:(18) přírůstek hmotnosti může být spojen především s léčbou VPA, VGB, ale i GBP, PGB, CBZ, naopak úbytek hmotnosti mohou působit TPM, ZNS, váhově neutrální jsou PHT, LTG, LEV, felbamát. Zastřešujícím pojmem pro rozvoj závažných rizik spojených s obezitou je metabolický syndrom X, s celým komplexem zdravotních odchylek (hypertenze, poruchy glykoregulace, ateroskleróza, prokoagulační stav, vyšší výskyt některých nádorů, psychické změny aj.).(33) Pohled na tuto potenciální rizikovost léčby se již vžil v psychiatrii, v epileptologii jakoby zůstával poněkud stranou.
Dalším tématem je léčba mladších i starších polymorbidních pacientů. Kromě výše zmíněných nevýhod může být antiepileptická léčba spojena s „žádoucími“ vedlejšími účinky léčby. Některá antiepileptika totiž mohou léčit i několik zdravotních poruch najednou – jedním lékem. Například u polymorbidního pacienta-diabetika s epilepsií, s algickou formou diabetické neuropatie s porušeným spánkem a s úzkostí můžeme pomocí „monoterapie“ PGB úspěšně léčit fokální epilepsii, bolestivou diabetickou neuropatii, úzkost a navíc účinně zlepšit spánek. PGB navíc nemá žádné významné interakce s dalšími farmaky (včetně warfarinu, antihypertenzív, hypolipidemik, antidiabetik). Obdobně můžeme pomocí TPM úspěšně léčit pacienta s epilepsií a migrénou, příznivě může být ovlivněna i případná nadváha či bolestivá neuropatie. Léčba LTG u polymorbidního pacienta s vaskulární epilepsií, s metabolickým syndromem X, s depresí, inhibicí či emoční nestabilitou je obvykle velmi dobře tolerovaná a vedle vlastní účinnosti na záchvaty nevykazuje významné lékové interakce. LTG je váhově neutrální, může mít antidepresivní účinky spojené s aktivací pacienta či se stabilizací jeho nálady.
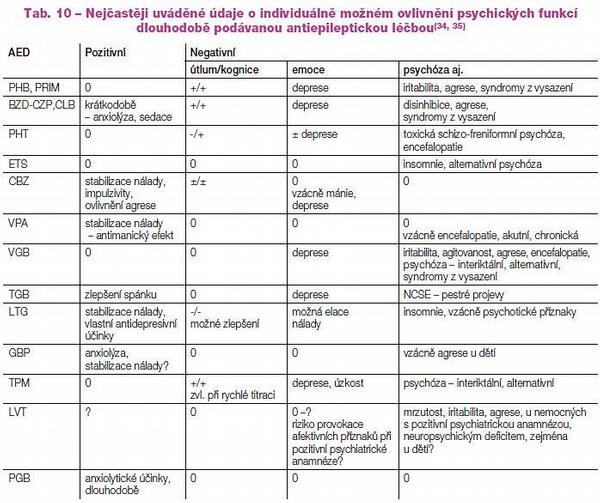
Tím přistupujeme k dalšímu aktuálnímu a důležitému tématu. Jsou jím psychotropní účinky antiepileptik.(34, 35) Vedle zmíněných tradičních nežádoucích účinků (útlum, kognitivní problémy) mohou antiepileptika individuálně vykazovat i specifické negativní psychotropní účinky: působit depresogenně (PHB, PRM, PHT, VGB aj.), event. způsobit iritabilitu, agitovanost, agresi, manické a psychotické příznaky. V současné době se pozornost zaměřuje i na využití pozitivních – žádoucích psychotropních účinků antiepileptik: ovlivnění úzkosti (PGB, GBP, CZP, CLB), deprese (LTG) a stabilizace nálady (LTG, CBZ, VPA, GBP) aj. Je o časté psychické poruchy, které postihují až polovinu pacientů s epilepsií. Souhrnný přehled potenciálních psychotropních účinků antiepileptik uvádíme v Tab. 10.
Oblastí, kde a jak antiepileptika ovlivňují interiktální stav nemocných, je samozřejmě více, než zde můžeme uvést, a bude jich jistě přibývat.
Závěr
Cílem sdělení bylo ukázat na to, že o volbě optimální antiepileptické léčby zdaleka nerozhoduje jenom typ epileptických záchvatů/syndromů. Z jedné strany ovlivňuje rozhodnutí navíc celá řada faktorů, týkajících se širších rizik a priorit konkrétních léků, z druhé strany řada faktorů tvořících konkrétní individualitu pacienta. Při volbě optimální antiepileptické léčby bychom dnes měli vždy vykročit dále, za záchvaty samotné. Máme k tomu dnes dostatek farmakologických prostředků.
Práce je podpořena výzkumným záměrem Patofyziologie neuropsychických onemocnění a její klinické aplikace VZ 0021620816.
Seznam citovaných léků a jejich zkratek:
CBZ – karbamazepin,
CLB – klobazam,
CZP – klonazepam,
BZD – benzodiazepiny,
ESL – eslikarbazepin,
GBP – gabapentin,
LCM – lacosamid,
LEV – levetiracetam,
LTG – lamotrigin,
OXC – oxkarbazepin,
PHB – fenobarbital,
PHT – fenytoin,
PGB – pregabalin,
PRM – primidon,
RFM – rufinamid,
STP – stiripentol,
SUL – sultiam,
TGB – tiagabin,
TPM – topiramát,
VGB – vigabatrin,
VPA – valproát, soli kyseliny valproové,
ZNS – zonisamid
O autorovi: Doc. MUDr. Jiří Hovorka, CSc.
Nemocnice Na Františku, Praha, Neurologické oddělení, neuropsychiatrické a epileptologické centrum Neurochirurgická klinika Ústřední vojenské nemocnice a 1. lékařské fakulty Univerzity Karlovy, Praha
e-mail: hovorka@nnfp.cz,
