Summary
Sutnar, A., Třeška, V., Liška, V., Šmíd, D., Skalický, T. The development of laparoscopy in liver surgery
The authors describe possibilities of using laparoscopy in liver diseases, more accurate diagnostics and higher efficacy of treatment for benign liver tumors. They also comment on possible difficulties in the diagnostics and treatment of both primary and secondary malignant liver tumors and evaluate the benefits of laparoscopic liver operations.
V posledním čtvrtstoletí zaznamenala chirurgie jater poměrně velký rozvoj a dosáhla výrazných úspěchů v léčbě benigních i maligních onemocnění jater. Tento trend byl způsoben nejen rozvojem nových technik a přístrojů, ale rovněž výrazným zlepšením peroperační a pooperační péče o tyto nemocné. Jako v každé chirurgické disciplíně se i zde prosazují nové miniinvazívní přístupy, které jsou v určitých případech výhodnější než přístup klasický – otevřený. Jedním z nejvýznamnějších miniinvazívních přístupů je laparoskopie, která se plně uplatňuje v chirurgii žlučových cest již od roku 1985, kdy byla poprvé provedena laparoskopická cholecystektomie.
U tohoto výkonu nahradil laparoskopický přístup z větší části přístup otevřený, který se však stále využívá u komplikací laparoskopie a v případech, jako jsou např. srůsty v dutině břišní, nepřehlednost v podjaterní krajině při těžké cholecystitidě nebo u nemocných s přidruženými chorobami, kteří nejsou schopni tolerovat nárůst nitrobřišního tlaku při kapnoperitoneu. Jak vzrůstala erudice chirurgů, kteří se věnují laparoskopii, a rozvíjí se technika a nástroje, bylo možno přistoupit k prvním laparoskopickým resekcím jater, jejichž rozsah se stále zvětšuje a kvalita výkonů stoupá. V současné době jsou na játrech laparoskopicky prováděny jak výkony menší, tak i rozsáhlé, jakými jsou například pravostranná hepatektomie či odběr části jater k transplantaci – split-resekce.(1)
Podmínky a vybavení
Chirurgií jater se zabývají většinou velká centra či úzce specializovaná pracoviště, protože pro dokonalý chod je nutné splnit řadu podmínek. Podstatný je tým chirurgů, kteří jsou schopni operovat játra laparoskopicky i otevřeným přístupem. V řadě případů je totiž nutné laparoskopický výkon převést na otevřený. Nedílnou součástí týmu je zkušený anesteziolog, radiolog a patolog. Anesteziolog musí rozumět dané problematice a dokonalou anestézií připraví pro chirurga ty nejlepší podmínky. Využití radiologa během operace je často nezbytné.
I když po určité době získá každý chirurg s prováděním peroperační sonografie (USG) určité zkušenosti a je schopen se dobře orientovat a využívat USG k lepšímu přehledu při resekcích jater, je nutné řadu patologických nálezů konzultovat právě s radiologem, který má v diagnostice rozhodně větší zkušenosti a může operatérovi pomoci při rozhodování o provedení výkonu cennou radou. Role patologa je zřejmá, když po odběru peroperační biopsie operatér čeká na výsledek, podle kterého se pak rozhodne o dalším postupu. Následná pooperační péče je u větších výkonů na játrech zajištěna na jednotce intenzívní péče (JIP), kam jsou nemocní převezeni rovnou z operačního sálu, a v případě rozsáhlejších výkonů mohou zůstat krátkodobě ventilováni.
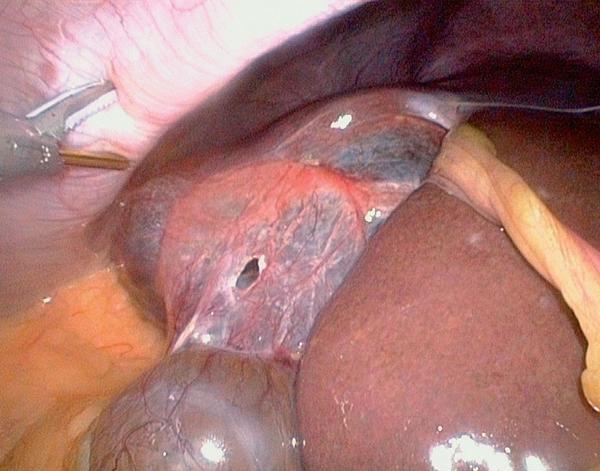
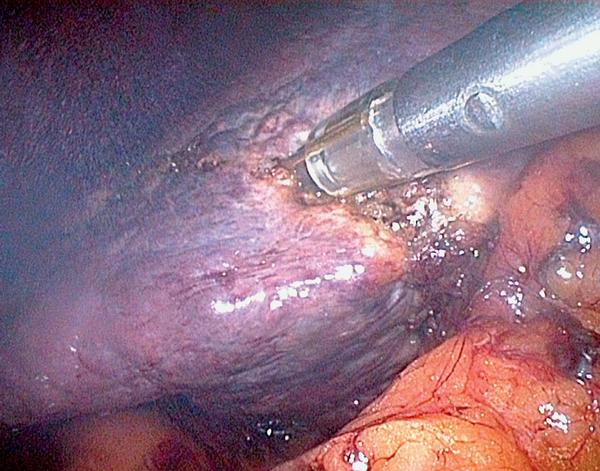
Další z podmínek je dostatečné přístrojové vybavení. Většina přístrojů, které jsou používány v jaterní chirurgii, se uplatňuje při obou přístupech – otevřeném i laparoskopickém. Díky tomu je možné při diagnostice využít laparoskopické USG sondy, při laparoskopických resekcích harmonický skalpel (Obr. 1), Ligasure nebo Habibovu laparoskopickou sondu. Harmonický skalpel či Ligasure se užívá k transekci jaterního parenchymu. Obě metody využívají ultrazvuk, který je převáděn na tepelnou energii. Tímto způsobem je tkáň koagulována a přerušena přímo nástrojem. Habibova sonda pracuje na principu radiofrekvenční ablace (RFA). RFA vytváří v tkáni koagulační nekrózu převedením vlnění na tepelnou energii pomocí speciálního generátoru vlnění a sondy, která je do tkáně aplikována. Standardně je využívána k přímému ošetření metastatických ložisek v játrech nevhodných k resekci.(2) U Habibovy sondy dochází ke koagulaci tkáně mezi čtyřmi jehlami. Zde vzniká koagulační nekróza, ve které je pak postižená část jater resekována (Obr. 2).
K ošetření krvácení z resekční plochy se s výhodou používá argonová koagulace či bipolární koagulace.
Některá pracoviště využívají u laparoskopických resekcí jater počítačem řízené robotické rameno, tzv. Ezop. Na tomto rameni je uchycena kamera, která reaguje na hlasový příkaz operatéra. Tím je zajištěn i u delšího výkonu stabilní obraz a lepší komfort celého týmu. Dalším krokem v laparoskopii je zavádění operačních robotů typu Da Vinci.(3) Do jaké míry se budeme ubírat touto cestou, však rozhodne až budoucnost. Už teď je ale zřejmé, že náklady na operování pomocí robotů jsou nesmírné a je otázkou, zda bude možné operovat i bez podpory grantových studií, které v současné době velkou část nákladů kryjí.
Přístup do dutiny břišní
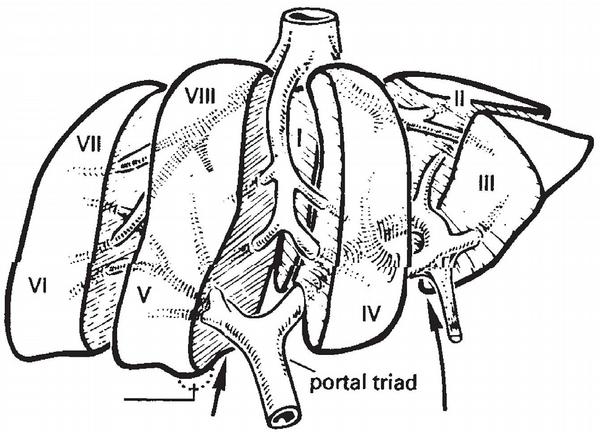
Jaký se volí u laparoskopie přístup a v jaké je nemocný poloze, záleží na uložení léze, kterou je třeba ošetřit. Játra a jejich rozdělení na segmenty jsou patrné na modelu (Obr. 3). Pro levostranné segmenty 2–3 a segmenty 4–6 je volena většinou poloha nemocného na zádech s nohama od sebe, kdy operatér stojí mezi nohama nemocného, asistence je z pravé strany nemocného.(4) Pro ložiska uložená dorzálně v segmentech 6 a 7 je výhodné nemocného uložit na levý bok, protože po uvolnění pravého triangulárního ligamenta je z tohoto přístupu možné ošetřit i pravou jaterní žílu a získat tak dobrý přehled o spojkách s dolní dutou žílou (DDŽ). Samozřejmě tato poloha není výhodná pro konverzi na otevřený výkon, protože je pak nutné nemocného přetočit na záda. Při aplikaci pracovních portů v této poloze hrozí, že budou zavedeny přes pravou pohrudniční dutinu.
S touto eventualitou je třeba počítat a operatér musí být připraven provést nemocnému v případě potřeby hrudní drenáž. Zda se během výkonu rozvíjí pravostranný pneumotorax, je zřejmé i klinicky podle stavu pravé poloviny bránice. Jaký přístup je volen u 8. segmentu, záleží na uložení ložiska. Podle grafických vyšetření je určeno, zda bude vhodné postupovat z ventrálního přístupu či nemocného natočit i se stolem na levý bok. K přístupu do dutiny břišní se standardně využívají při diagnostice 2–3 porty, u resekcí většinou 4–6 portů. Je výhodné, aby u resekcí směřoval nástroj přímo do resekční linie, kterou je postupováno. Pokud operatér ví, že bude ložisko ošetřovat pouze pomocí RFA, využije u segmentů 7 a 8 transtorakální přístup a za použití videotorakoskopie (VTS) ošetří ložisko přes bránici.
Technika resekcí – Pringleho manévr a HALS
Pro jaterní resekce je využívána buď přímá, nebo 30stupňová optika. U menších resekcí, rozsahem řádově do segmentektomie, se většinou pouze zajistí hepatoduodenální ligamentum, aniž by bylo nutné ho uzavřít. Uzávěr ligamenta, tzv. Pringleho manévr,(5) se využije pouze v případě krvácení, aby bylo možno resekci laparoskopicky dokončit, krvácení zastavit či zmírnit a následně ošetřit. Pokud se krvácení zastavit nedaří, je nezbytné převést výkon na laparoskopicky asistovaný či otevřený a vzniklé krvácení ošetřit touto cestou. Pringleho manévru se využívá i u rozsáhlejších jaterních resekcí ke zmenšení krevních ztrát. Většinou přistupujeme k přerušovanému uzávěru, kdy se na 20 minut uzavře průtok hepatoduodenálním ligamentem a pak se na 5 minut znovu obnoví.
Je totiž prokázáno, že intermitentním uzavřením průtoku dochází k daleko menšímu hypoxickému poškození hepatocytů než při uzavření kontinuálním, které může u zdravých jater trvat 60–75 minut. U jater změněných cirhózou či steatofibrózou je třeba dobu ischémie zkrátit přibližně na polovinu. Vyhneme se tím možnému jaternímu selhání, které se může rozvinout v pooperačním období. Při využití intermitentního uzávěru se může čas ischémie ještě mírně prodloužit až na cca 90 minut. K uzavření průtoku krve hepatoduodenálním ligamentem se používá většinou gumová hadička či tkanice, která je pomocí disektoru protažena kolem ligamenta.
Po nasazení turniketu a zatažení je zajištěna nějakým nástrojem či klipem a v pravidelných intervalech je průtok ligamentem obnovován. Stejně tak je možné využít k přerušení krevního toku přes hepatoduodenální ligamentum do jater snímatelné laparoskopické svorky, které jsou aplikovány pomocí speciálního klipovače. Přerušení průtoku hepatoduodenálním ligamentem je občas možné se vyhnout cílenou preparací v jaterním hilu a ošetřením jednotlivých struktur. Většinou je nutné provést cholecystektomii, aby byl přehled v jaterním hilu dostatečný.
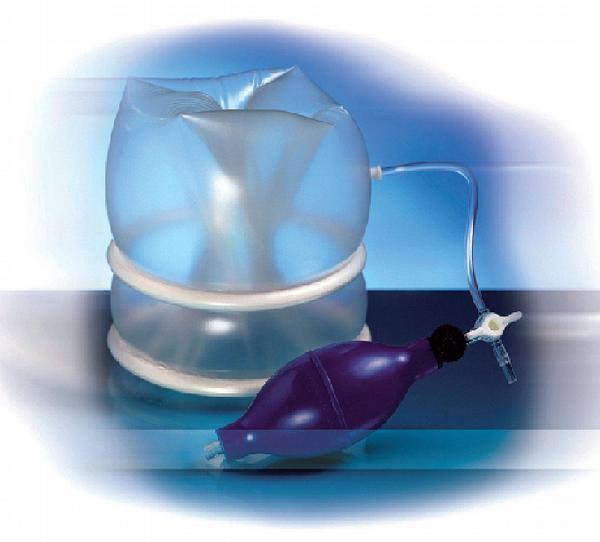
Při řešení krvácení byl zmíněn laparoskopicky asistovaný přístup, který je znám rovněž pod termínem HALS (hand-assisted laparoscopy – manuálně asistovaná laparoskopie). Tato metoda využívá různé systémy sterilního disku, jako jsou Gelport, Omniport či LapDisk (Obr. 4, 5), který je zaveden do břišní stěny malou laparotomií a je schopen udržet kapnoperitoneum. Skrz tento disk může chirurg zavést do dutiny břišní nástroj či ruku a využít tohoto přístupu k ozřejmení krvácení. Pomocí HALS je možno vzniklé krvácení lépe ošetřit a eventuálně účinně zatampónovat před případným převedením výkonu na otevřený. Kromě řešení komplikací je metoda HALS používána u obézních nemocných a při nepříznivém uložení lézí v játrech. Ruka jako nástroj výrazně usnadňuje preparaci, protože si operatér může játra natočit tak, aby po jejich uvolnění získal dostatečný přehled i přístup k resekované části. Díky tomuto přístupu je také snadnější dodržet bezpečnostní lem u resekcí malignit.
Využití ultrazvuku a radiofrekvence
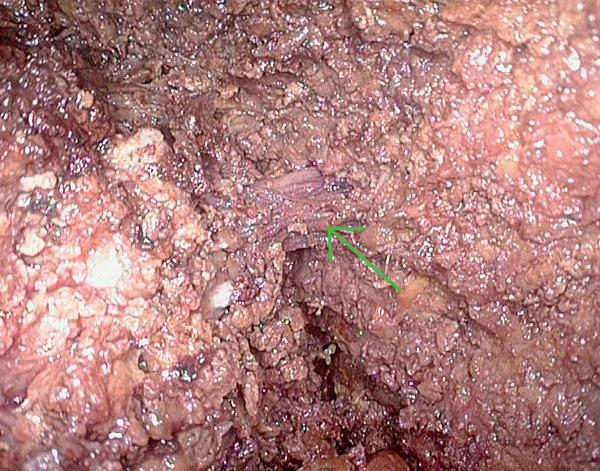
Podle uložení ložiska se provádí mobilizace určité části jater, kdy jsou přerušeny závěsy, jako jsou ligamentum teres hepatis, levé či pravé ligamentum triangulare nebo ligamentum falciforme hepatis. Většinou se přitom používá harmonický skalpel. Ten má své místo i při vlastní resekci jater. Používá se spolu s bipolární koagulací na transekci jaterního parenchymu, kdy se postupuje ve vytyčené resekční linii a ozřejmují se větší cévní a žlučové struktury. Ty jsou pak ošetřeny podvazy či zajištěnými klipy. Na segmentární a větší cévy nebo žlučovody (Obr. 6) se většinou používá cévní stapler. Ke stavění krvácení z resekční plochy je možno využít kromě bipolární ještě argonovou koagulaci. Kromě přístrojů ke stavění krvácení se dále u laparoskopických resekcí osvědčuje používání hemostyptických materiálů na bázi fibrinu, např. fibrilárního Sufgicelu.
Tento materiál je schopen zastavit i úporné krvácení z jaterního parenchymu, pokud není v portálním řečišti či řečišti (DDŽ) výraznější přetlak. Při laparoskopii je možné použít k transekci jaterního parenchymu také Ligasure. Pracuje na podobném principu jako harmonický skalpel a záleží na operatérovi, který nástroj mu lépe vyhovuje. Další možností, jak provádět laparoskopickou resekci jater, je aplikace Habibovy sondy, která využívá, jak bylo zmíněno výše, radiofrekvenční energii.(6) Postupným zapichováním čtyřhrotové sondy do jaterního parenchymu vytváří operatér v určité linii koagulační nekrózu, ve které pak postiženou část jater resekuje. Rovněž při resekci jater pomocí Habibovy sondy je dobré ošetřit segmentární cévy a žlučovody pomocí cévního stapleru.
K dokonalému přehledu o těchto strukturách využívá operatér opět peroperační USG. Při zapichování Habibovy sondy do jater existuje riziko poranění nějaké cévy, která nemusí být koagulací dostatečně ošetřena, a může tak dojít k závažné komplikaci ve smyslu krvácení, která může skončit konverzí výkonu. Je proto vhodné v místech, kde jsou přítomny cévní struktury, využívat možnosti pouze částečného vysunutí hrotů z laparoskopické Habibovy sondy. K přesnější preparaci kolem nich se pak použije harmonický skalpel, Ligasure či bipolární koagulace. Tento příklad ukazuje, že je optimální, když může chirurg využívat při jedné laparoskopické resekci více přístrojů podle aktuální potřeby.
Kromě využití RFA k resekci jaterního parenchymu (Habibova sonda) je možné pomocí RFA ošetřit laparoskopicky ložiska v játrech přímo. Důvodů k tomuto postupu je celá řada. Může to být rozložení ložisek v jaterním parenchymu, celkově špatný stav nemocného, který by větší resekční výkon nepřežil, nebo špatný stav jater, který dovoluje pouze co nejmenší výkon, aby nedošlo k jaternímu selhání. Takovýmto příkladem je hepatocelulární karcinom (HCC) v jaterní cirhóze.(7) Pokud je ložisko v játrech uloženo vysoko pod bránicí, je výhodnější použít místo laparoskopie VTS a ošetřit ložisko v játrech přes bránici. U nedokonale ošetřených ložisek pomocí RFA dochází k tzv. „non-ablaci“. To znamená, že ložisko v játrech nebylo postiženo celé a bude pokračovat ve svém růstu.
Zde je rozhodující laparoskopicky peroperačně provedená sonografie, která přesně ložisko změří a pomocí které se přesně zacílí RFA-sonda do jaterního parenchymu. Hovoří se o RFA pod USG kontrolou. Tento postup umožní najít nejvhodnější cestu k ložisku, které chceme pomocí RFA ošetřit. Platí to i pro ložiska patrná na povrchu, protože i ta se mohou šířit do okolí a zasahovat různě hluboko do jater. Díky USG je možné zhodnotit dokonale anatomii cévního i žlučového stromu a vyhnout se tak strukturám, které nesmí být poraněny. RFA je schopna vytvořit koagulační nekrózu do velikosti 5 cm, proto by velikost ložiska ošetřovaného pomocí RFA neměla překročit 4 cm, aby bylo možné kolem zachovat alespoň 0,5 cm bezpečný lem.(8)
U větších ložisek, kolem 5 cm, je nutné aplikovat RFA sondu několikrát či využít 2–3 sond současně. Riziko non-ablace je však v takových případech větší a je třeba s ním počítat. V takových případech se hovoří o pouhém zmenšení nádorové masy – cytoredukci, což se s výhodou využívá například u karcinoidu, který je semimaligní a většinou reaguje dobře na podávanou adjuvantní chemoterapii. Po jejím dokončení se může znovu přistoupit k RFA a rezidua tumoru znovu ošetřit. U maligních nádorů tento postup indikován není, protože i přes podanou chemoterapii se nedostavuje požadovaný efekt. Jak byla RFA úspěšná, se kontroluje pomocí CT jater, nejdéle druhý den po výkonu. V závěru části o RFA je třeba zdůraznit, že tato metoda je pouze metodou doplňkovou k resekční terapii, protože – jak bylo zmíněno výše – při non-ablaci hrozí vysoké riziko recidivy a pouze resekce je brána jako léčba kurativní. Proto je RFA aplikována pouze u nemocných, kteří nejsou schopni podstoupit z jakéhokoliv důvodu resekci jater.
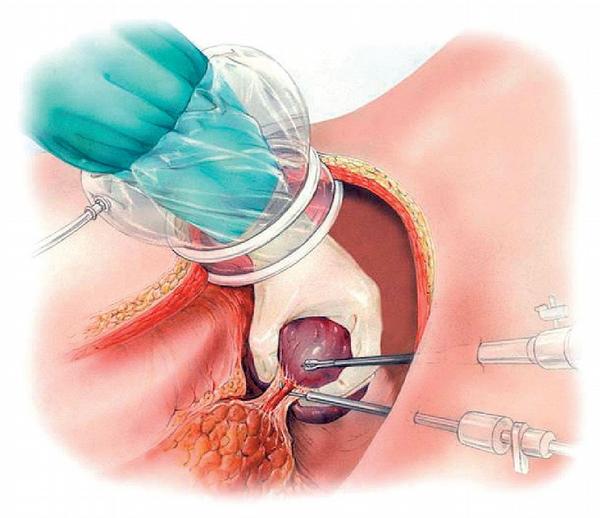
Využití laparoskopie v jaterní chirurgii
V chirurgii jater se tedy laparoskopie uplatňuje v široké míře. Je využívána jak u výkonů akutních, jako jsou traumata jater, tak u výkonů elektivních. V obou případech se využívá jako metoda diagnostická nebo metoda léčebná. U traumat je využití menší než u elektivních výkonů, protože při poranění jater bývají obvykle poraněny i další orgány, nemocný může být oběhově nestabilní a my přesně nevíme, odkud krvácí. Je třeba zdůraznit, že v žádném případě nejsou indikováni k laparoskopické revizi oběhově nestabilní pacienti. K diagnostické laparoskopii se přistupuje po traumatu dutiny břišní, u oběhově stabilního nemocného, kdy je podezření na poranění v dutině břišní při zhoršování klinického nálezu na břiše, či jsou přítomny známky krvácení do dutiny břišní prokázané grafickými metodami.
Nejlépe je ilustrovat takové situace příklady. U oběhově stabilního nemocného po úrazu s podezřením na trauma jater, kdy při grafických vyšetřeních přibývá tekutina (krev) v dutině břišní, je vhodné přistoupit k diagnostické laparoskopii. Stejně tak u nemocného, který je sledován pro hemoperitoneum, při podezření na poranění jater a během hospitalizace je nutné podat opakované krevní převody a nemocný zůstává oběhově stabilní, tak i v tomto případě je možné provést laparoskopickou revizi dutiny břišní. V případě nevelkých trhlin jater, které jsou uloženy povrchově, je optimální přiložit hemostyptické materiály nebo využít argonovou koagulaci k zastavení krvácení. U hlubších trhlin je vhodné použít RFA a zdroj krvácení zastavit aplikací RFA sondy do místa krvácení.
I zde je využito tepelné energie ke koagulaci tkáně, ale v hloubce jaterního parenchymu. Může se stát, že grafické metody neodhalí rozsáhlejší poranění jater, které je odhaleno až při laparoskopické revizi. V takovém případě je nutné převést rychle výkon na otevřený, zbytečně neztrácet čas, pokusit se krvácení co nejdříve zastavit a nesnižovat nemocnému šanci na přežití. Jakým způsobem ošetří operatér větší poranění jater, závisí na typu poranění, celkovém stavu nemocného a zkušenostech samotného operatéra. Může pouze založit tamponádu kolem jater nebo provést až resekci jednoho z laloků jater. Tím se ale dostáváme daleko od laparoskopie. Podstatné je zde zdůraznit, že i u traumat jater má laparoskopie své místo a nemocní z tohoto postupu, pokud je správně indikován, profitují. Laparoskopie je totiž tolik nezatíží a pooperační průběh je lehčí. Pokud mají sdružené poranění hrudníku, není ovlivněna mechanika dýchání jako například po laparotomii. Stejně tak se rychleji obnovuje pasáž gastrointestinálním traktem (GIT).
U elektivních výkonů jsou indikační kritéria laparoskopie širší. Při diagnostice nám slouží především v případech, kdy selhaly grafické zobrazovací metody (typu ultrasonografie – USG, computerové tomografie – CT, magnetické rezonance – MR atd.) a nejsou schopné dát nám jasnou odpověď, jaký útvar se v játrech nachází. Zde nastupuje laparoskopie jako metoda volby. Využívá se k přímému ohledání nálezu na játrech, kdy se provádí peroperačně USG pomocí laparoskopické USG sondy a v nejasných případech se odebírá z procesu na játrech i biopsie. Biopsie je odebrána punkčně pomocí speciální jehly, nebo je přímo vyříznuta část patologického jaterního parenchymu. Podle peroperační biopsie či USG nálezu je pak možné přistoupit rovnou k ošetření ložiska na játrech, a to jak laparoskopicky, tak otevřeně. I zde si je však třeba uvědomit, že je nutné mít v tomto směru určité zkušenosti a při ohledání příslušného nálezu postupovat dostatečně pečlivě.
Jak uvádí ve své práci Hsu, při laparoskopii je možné přehlédnout obtížněji přístupná ložiska, a proto i zde je nutné zvažovat v nerozhodných případech a u podezření na malignitu laparoskopicky asistovaný či otevřený přístup s využitím hmatu k ohledání podezřelé léze.(9) Léčebně se používá laparoskopický přístup u benigních onemocnění jater, jako jsou jaterní cysty, fokální nodulární hyperplazie (FNH), hemangiom a jaterní adenom. U jaterních cyst, hemangiomů a FHN jsou nemocní indikováni k laparoskopickému ošetření v případě vyjádřené symptomatologie. U jaterních adenomů je nemocným proveden výkon v brzké době po stanovení diagnózy, protože tento nález je hodnocen jako prekanceróza. Z adenomu se může vyvinout v řadě případů HCC; tato transformace je daleko pravděpodobnější, jestliže je adenom větších rozměrů.
U prostých jaterních cyst je prováděna většinou fenestrace cysty s odběrem biopsie stěny a evakuací tekutiny, kterou cysta obsahuje.(10) V případě histologického nálezu cystadenomu či cystadenokarcinomu je doplněna enukleace či resekce zbytků cysty.(11) Zde je možný opět laparoskopický přístup. Při nevhodné lokalizaci je nemocný operován otevřeně. FNH, hemangiom či adenom je možné ošetřit rovněž enukleací, kdy se postupuje po povrchu nádoru a zachovává se okolní jaterní parenchym.(12) Tento postup je vhodný u lézí povrchově uložených. U tumorů uložených intraparenchymatózně je většinou nutné provést jaterní resekci v nezbytně nutném rozsahu.
U maligních onemocnění jater je laparoskopie rovněž využívána ve stále větší míře, nicméně její role je zde z několika důvodů diskutována. Laparoskopicky jsou ošetřovány primární i sekundární tumory jater. Mezi primární tumory patří HCC a cholangiocelulární karcinom (CHCC). Jejich výskyt je v našich zeměpisných šířkách daleko vzácnější než např. v Asii či Africe. Tvoří cca 20 % nádorů jater. Častější jsou v naší zemi tumory sekundární a z nich jsou v 80 % zastoupeny metastázy kolorektálního karcinomu (KRK). Naše republika je totiž ve světě na prvním místě ve výskytu KRK, který metastazuje až v 60 % případů do jater.(13) Ve zbylých 20 % sekundárních nádorů, které metastazují do jater, jsou zastoupeny nádory ledvin, prsu, ostatního zažívacího ústrojí (žaludku či pankreatu), gynekologické nádory, nádory štítné žlázy, semimaligní karcinoid a vzácně i další nádory.
Laparoskopicky jsou dnes prováděny výkony typu metastazektomie, neanatomické jaterní resekce, segmentektomie až po lobektomie či hepatektomie. Právě otázka přístupu a rozsahu výkonu při ošetřování malignit jater je však místem, kde se střetávají různé názory a úhly pohledu. Jak ukazují zkušenosti a porovnání u menších jaterních resekcí až do rozsahu segmentektomie, zdá se pro nemocného výhodnější laparoskopické ošetření. Polignano ve své práci udává, že při laparoskopii v rozsahu segmentektomie se dosahuje menších krevních ztrát, operační čas je kratší, stejně jako doba hospitalizace, a rovněž náklady spojené s celkovou chirurgickou léčbou jsou nižší.(14) Tento názor podporuje Tsinberg, kdy srovnává laparoskopický a otevřený přístup u wedge resekcí, segmentektomií a neanatomických resekcí jater.(15)
Z jeho práce vyplývá, že u otevřených resekcí jsou nuceni častěji klampovat hepatoduodenální ligamentum a mají větší krevní ztrátu, při laparoskopii je sice delší operační čas, ale u nemocných se dříve obnovuje pasáž GIT a hospitalizační doba je kratší. Udává, že u obou použitých metod dosahují stejných výsledků v dodržení bezpečnostního lemu ve zdravé tkáni od tumoru. Nguyen při srovnání obou přístupů dospěl k závěru, že u laparoskopického přístupu mají nemocní lehčí pooperační průběh, ale hrozí riziko konverze pro krvácení a rovněž operační čas je delší.(16) Na druhou stranu Gamblin podle svých zkušeností hodnotí laparoskopii jako velmi přínosnou pro resekci benigních cyst, ale pro malignity preferuje otevřený přístup.(17)
Robles není přesvědčen o laparoskopii jako o metodě, která je schopna provést dostatečný staging.(18) Využívá laparoskopicky asistovaný přístup (HALS), který nazývá „zlatým standardem“ a staví ho na stejnou úroveň jako přístup otevřený. Ruku zavedenou do dutiny břišní využívá k palpaci, a tím k ověření nálezu. Disk je možné také použít k zavedení nástroje nebo se dá využít na konci operace k odstranění preparátu z dutiny břišní. Pokud je preparát větších rozměrů, např. u pravostranné hepatektomie, rozšíří se provedená laparotomie po disku a preparát se odstraní touto cestou. Pokud jsou játra resekována pouze laparoskopicky, je nutné k odstranění většího preparátu z dutiny břišní provést laparotomii. Je možné volit laparotomii střední a využít tak částečně přístup po portu, nebo provést Pfannenstielův řez v podbřišku. V obou těchto případech však odpadá hlavní výhoda laparoskopie – miniinvazivita, a je tedy na zvážení, zda rozsáhlejší výkony k laparoskopii indikovat.
Závěr
Z těchto několika příkladů je patrné, že laparoskopie si již vybudovala dostatečně pevnou pozici i v jaterní chirurgii. Svou významnou roli bude zcela jistě dále hrát v diagnostice a ošetřování benigních lézí jater. U maligních onemocnění jater je zřejmé, že budou proti sobě stále stát laparoskopie a otevřený přístup. Pro laparoskopii hovoří kratší hospitalizační doba, dříve obnovená pasáž GIT a celkově kratší rekonvalescence nemocného, charakteristiky stejné i u ostatních laparoskopických výkonů v dutině břišní. Relativní je délka výkonu, která se samozřejmě zkracuje se zkušenostmi operatéra a celého týmu. Otázkou u malignit však je dostatečnost resekčního výkonu a dokonalá explorace dutiny břišní. Zde je na zvážení laparoskopicky asistovaný přístup, který umožňuje využití ruky jako nástroje a je velmi dobrou alternativou mezi oběma přístupy. Výhody laparoskopie jsou pak sporné u velkých resekcí, kdy odstraňujeme jeden z jaterních laloků a jsme nuceni doplnit k vyjmutí preparátu laparotomii.
Závěrem je nutné zdůraznit, že je na každém chirurgovi, aby posoudil vhodnost metody a přínos pro nemocného individuálně, protože je evidentní, že pomocí laparoskopie, kterou využívá zkušený chirurgický tým, je možné provést bezpečně i rozsáhlé jaterní resekce.
Článek vznikl s podporou výzkumného záměru VZ MSM 0021620819 a grantu IGA MZ ČR 9731–4.
O autorovi: MUDr. Alan Sutnar, Ph. D., prof. MUDr. Vladislav Třeška, DrSc., MUDr. Václav Liška, Ph. D., MUDr. David Šmíd, doc. MUDr. Tomáš Skalický, Ph. D.
Univerzita Karlova v Praze, Lékařská fakulta a Fakultní nemocnice Plzeň, Chirurgická klinika
e-mail: sutnar@fnplzen.cz











