Primárním cílem projektu bylo nalézt odpověď na otázku „co dělat v případě, že první léčebná metoda selže“. Léčba probíhala v systému „measurementbased care“ – péči založené na měření. Hlavním kritériem úspěšnosti léčby bylo dosažení plné remise. Výsledky studie STAR*D potvrzují, že současná medicína dokáže většině těchto nemocných velmi výrazně pomoci. Zlatým pravidlem léčby depresivní epizody je v současné době sekvenční podávání moderních antidepresiv v kombinaci s psychoterapií.
Summary
Raboch, J. News in the treatment of depression – what we learned from STAR*D study The STAR*D study included 4,041 individuals suffering from non-psychotic major depressive disorder, who were treated in 23 psychiatric and 16 primary care settings. The primary objective of this project was to find an answer to the question „what to do in case first therapeutic method fails”. Treatment took place in a „measurement-based care” – care based on measurement system. The main criterion for success of treatment was the achievement of full remission. The results of STAR*D study confirm that current medicine can greatly help most of these patients. Currently sequential administration of modern antidepressants in combination with psychotherapy is the golden rule for treatment of a depressive episode.
Od roku 2001 se můžeme průběžně seznamovat s výsledky zatím největší studie na poli léčby afektivních poruch – STAR*D (Sequenced Treatment Alternatives to Relieve Depression – Sekvenční alternativy léčby deprese), která byla zorganizována americkým Národním institutem pro duševní zdraví (NIMH). Do studie bylo zařazeno 4041 jedinců trpících nepsychotickou formou velké deprese, kteří byli léčeni ve 23 psychiatrických ambulancích a 16 ordinacích praktických lékařů. Pacienti byli zdravotně pojištěni jak státem, tak soukromě. Autoři jsou přesvědčeni, že se jednalo skutečně o naturalistickou studii v běžné klinické praxi.
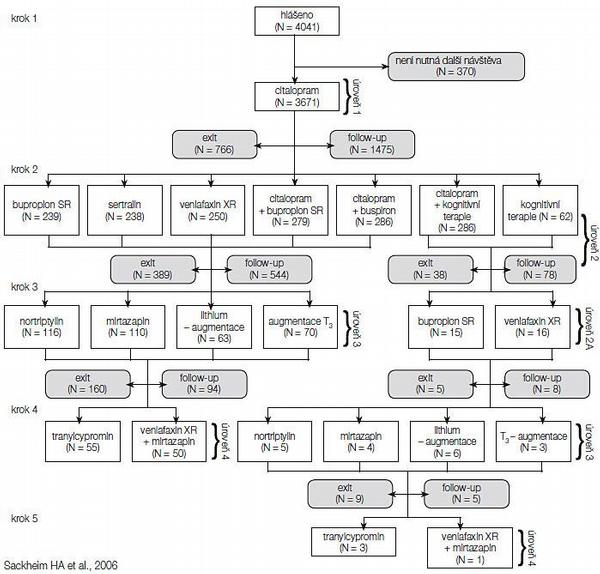
Primárním cílem projektu bylo nalézt odpověď na otázku „co dělat v případě, že první léčebná metoda selže“. Léčba probíhala v systému „measurement-based care“ – péči založené na měření. To znamená, že byly rutinně používány posuzovací škály měřící výsledek léčby, systematicky byly monitorovány její vedlejší účinky a antidepresivní léčba farmakologická i psychoterapeutická probíhaly podle standardního algoritmu v potenciálně čtyřech léčebných krocích (schéma postupu – viz Obr. 1). V průběhu minimálně ročního sledování pacientů byla využita většina v současné době dostupných antidepresiv (látky typu SSRI, SNRI, NaSSA, NDRI, TCA, IMAO) jak v monoterapii, tak v kombinaci (venlafaxin s mirtazapinem, citalopram s bupropionem), jejich účinek byl potencován buspironem, lithiem a T3. Byla použita také kognitivně-behaviorální psychoterapie (KBT). Z dostupných standardních léčebných prostředků u terapeuticko-rezistentních pacientů nebyly použity pouze elektrokonvulze.
Hlavním kritériem úspěšnosti léčby bylo dosažení plné remise. Ta byla definována v 17položkové Hamiltonově škále pro depresi (HAMD-17) jako skóre nižší než 8. K měření výsledků byla použita i sebeposuzovací škála QIDS-SR (Quick Inventory of Depressive Symptomatology-Self-Report, remise definována jako skóre nižší než 6). Pakliže došlo k dosažení remise, bylo pacientovi navrženo, aby pokračoval v úspěšné léčbě po dobu 12 měsíců. V této observační fázi pak byla sledována častost event. relapsů deprese. Osoby, u kterých se po 12–14 týdnech léčení remise nedostavila, dostaly možnost terapie následujícím krokem.
Při výběru pacientů pro jednotlivé léčebné postupy byla použita tzv. rovnovážná stratifikace, která zajistila, že pacient nebude léčen takovou metodou, která je pro něj primárně nepřijatelná. To znamenalo např., že si pacienti mohli zvolit, zda v následujícím kroku budou léčeni záměnou antidepresiva nebo jeho augmentací. Jedincům, kteří preferovali psychoterapii, byla nabídnuta pouze KBT.
V prvním kroku studie STAR*D byli všichni pacienti léčeni monoterapií citalopramu flexibilně dávkovaného od 20 mg do 60 mg v průměru 41,8 ± 16,9 mg denně na konci terapie. Pozitivní klinické odpovědi (50% pokles skóre posuzovací škály) bylo dosaženo u 47 % a remise u 28 % léčených nejčastěji mezi 6. a 12. týdnem léčby. S dosažením remise pozitivně korelovaly takové faktory, jako zda je pacient běloch, žena, má zaměstnání, je lépe vzdělán či má vyšší příjem. Negativní prognostické faktory byly delší trvání depresivní epizody, psychiatrická i somatická komorbidita. Již v prvním kroku se tedy výrazně zlepšil duševní stav u poloviny pacientů a u více než jedné čtvrtiny bylo dosaženo prakticky vymizení psychopatologických příznaků! To je jistě slušný výsledek, avšak je třeba mít na zřeteli, že u většiny léčených kýženého cíle – remise – nedosáhneme. Proto „sekvenční léčba“ je u pacientů s depresí v naší klinické praxi skutečně nezbytná!
Neúspěšně léčení si ve druhém kroku mohli zvolit mezi záměnou antidepresiva či jeho augmentací. Při záměně na bupropion SR (průměr 282,7 ± 104,4 mg/den) došlo k remisi u 21 % léčených, v případě monoterapie sertralinem (135,5 ± 57,4 mg/den) u 18 % a venlafaxinem (193,6 ± 106,2 mg/den) u 25 %. Mezi léčebnými výsledky ani tolerabilitou léčby nebyly shledány statisticky významné rozdíly. Zjištěná fakta neposkytují důkazy pro to, že by záměna antidepresiva za jiné s rozdílným mechanismem účinku byla efektivnější než záměny mezi jednotlivými látkami typu SSRI.
U druhé skupiny byl citalopram augmentován bupropionem SR (267,5 ± 99,8 mg/den) nebo buspironem (40,9 ± 16,7 mg/den). Opět míra remise u obou podskupin byla přibližně stejná – 29,7 %, resp. 30,1 %. V případě bupropionu však bylo dosaženo ve srovnání s buspironem většího zlepšení na škále QIDS a ukončení léčby pro intoleranci bylo méně časté. To tedy favorizuje augmentaci látkou typu NDRI.
Celkově se dá říci, že dosažení remise ve druhém kroku se dostavilo u další čtvrtiny léčených. Součet dosažených remisí v prvém a druhém kroku se tedy pohybuje mezi 50–55 %. Častěji dosáhli remise ti, kteří v prvním kroku alespoň částečně reagovali na léčbu citalopramem, měli méně komorbidních zdravotních obtíží a byli v lepším sociálním postavení.
KBT psychoterapie byla aplikována po rezistenci na citalopram buď samostatně, nebo jako jeho augmentace. Pouze asi jedna třetina pacientů souhlasila s použitím psychoterapie jako jediného způsobu léčení. Míra dosažené remise při terapii KBT byla obdobná jako u léčených psychofarmaky (25,0 %, resp. 27,9 %). Její dosažení bylo rychlejší při kombinaci s farmaky než při monoterapii KBT, avšak v těchto případech bylo spojeno s více nežádoucími účinky. Psychoterapie deprese přináší tedy stejně kladné účinky jako antidepresiva, je lépe snášena než psychofarmakoterapie, avšak pro pacienty je jako monoterapie méně důvěryhodná. Ve třetím kroku byly v monoterapii použity mirtazapin (42,1 ± 15,7 mg/den) a nortriptylin (96,8 ± 41,1 mg/den); k remisi došlo u 12 %, resp. 20 % pacientů. Jako augmentační preparáty byly nasazeny lithium (859,8 ± 373,1 mg/den) a T3 (45,2 ± 11,4 mikrog/den) a k remisi došlo u 16 %, resp. 25 % léčených. Nebyly zjištěny signifikantní rozdíly mezi jednotlivými podskupinami v dosažení remise. Tolerabilita jednotlivých druhů medikace se nelišila s výjimkou lithia. Nežádoucí účinky zde byly statisticky významně častější ve srovnání s T3 (p = 0,045) a více pacientů na lithiu ve srovnání s T3 (23,2 %, resp. 9,6 %) ukončilo z tohoto důvodu léčbu. Potvrzuje se tedy, že i u nás málo používaná augmentace antidepresivní léčby tyreoidálními hormony je pro pacienty vhodná a méně zatěžující ve srovnání s lithioterapií.
Ve čtvrtém kroku byla nasazena a porovnána léčba tranylcyprominem (36,9 ± 18,5 mg/den, remise v 7 %) a kombinací venlafaxinu (210,3 ± 95,2 mg/den) s mirtazapinem (35,7 ± 17,6 mg/den, remise ve 14 %). Efektivita obou postupů se signifikantně nelišila, ale podávání IMAO bylo spojeno s vyšší častostí přerušení léčby pro nesnášenlivost. Přitom u tranylcyprominu bylo třeba dodržovat dietní omezení. Tato zjištění poukazují na výhody kombinace moderních antidepresiv u farmakorezistentních nemocných ve srovnání s u nás již prakticky nedostupnými látkami IMAO.
Compliance je velmi významným faktorem dlouhodobé léčby nemocných s potenciálně chronickou chorobou, jakou je i deprese. Ve studii STAR*D 26 % léčených ukončilo léčbu z nemedicínských důvodů. Ihned po zahájení léčby tak učinilo 34 % z nich, do 3 měsíců 59 % a později dalších 7 %. Jednalo se o mladší pacienty s nižším vzděláním, s pocity lepšího mentálního fungování. Naopak lidé, kteří zažili více depresivních epizod, měli tendenci lépe spolupracovat.
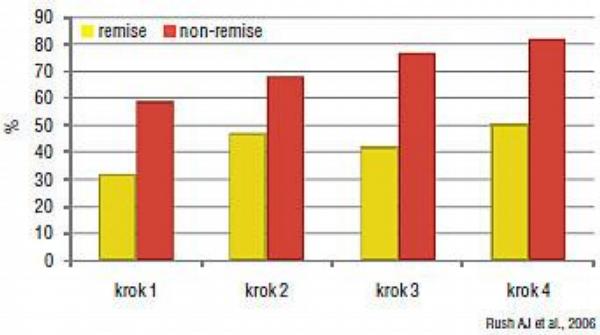
Nálezy STAR*D potvrzují klinické zkušenosti, že pravděpodobnost dosažení remise po prvních neúspěšných léčebných pokusech se zmenšuje. V dohledu je přitom již další meta, a to dosažení „well being“ včetně normálního psychosociálního fungování. Celková míra remisí byla v jednotlivých krocích 28 %, 25 %, 18 % a 10 %. To ale také znamená, že po dvou krocích dosáhneme při dobré péči remise u 53 % a po čtyřech v 81 %. To skutečně není špatný výsledek.
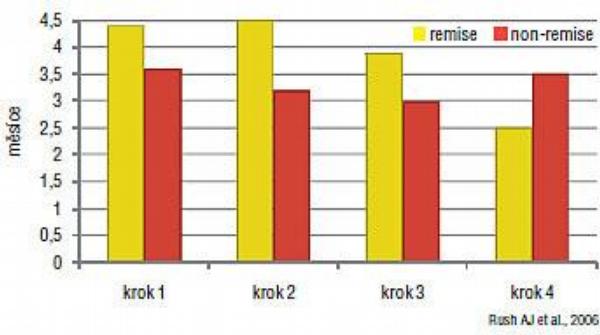
Bylo potvrzeno, že dosažení plné remise je správným hlavním cílem naší léčby. Nemocní, kteří dosáhli remise v jednotlivých krocích, měli nižší pravděpodobnost relapsu depresivní poruchy v následujícím roce než ti, kteří plné remise nedosáhli (Obr. 2), a čas objevení se relapsu byl u nich kratší (Obr. 3). To potvrzuje známou skutečnost, že reziduální symptomy jsou velmi významným negativním prognostickým faktorem a je třeba se velmi agresivně snažit je odstranit již v akutní etapě antidepresivní léčby.
STAR*D nemohla odpovědět na klinicky závažnou otázku, zda je lepší při neúspěchu prvé léčebné metody primární lék vyměnit, nebo augmentovat. Metodika použité randomizace to neumožnila. Při tomto rozhodování se asi budeme dále řídit tím, zda došlo alespoň ke klinické odpovědi. Zde je vhodné augmentovat. Tam, kde ke klinické odpovědi nedošlo, je lepší lék zcela vyměnit.
Z těchto výsledků plyne více poučení. Mnoho pacientů, kteří jsou označeni jako rezistentní, jsou ve skutečnosti pouze pseudorezistentní. Jen u nich nebylo využito všech léčebných možností, které nám současná praxe a doporučené standardy péče nabízí. Ve všech případech antidepresivní léčby je třeba využít celou kapacitu podávaného léku jak v maximalizaci dávky, tak v délce jeho podávání. Zde se doporučení ze studie STAR*D částečně rozcházejí s některými nejnovějšími stanovisky. Autoři STAR*D zdůrazňují minimální dobu podávání 4–6 týdnů s tím, že někdy je třeba podávat lék ještě déle. Jiné studie však poukazují na tu skutečnost, že když nedojde k výrazné klinické změně do 2 týdnů léčby, je pravděpodobnost úspěchu při dalším podávání podstatně snížena. V těchto konkrétních případech je doporučeníhodné se řídit aktuálním duševním stavem pacienta, jeho postojem k léčbě a její snášenlivostí. Studie STAR*D se zabývala i některými dalšími charakteristikami jedinců trpících depresivní epizodou. Bylo prokázáno, že nejen biologické vlivy, jako jsou pohlaví, rasa, celková nemocnost či délka deprese, ale také psychosociální faktory, jako jsou např. rodinný stav, zázemí přátel, stupeň vzdělání, zaměstnání, finanční výdělek, zdravotní pojištění či dosavadní kvalita života, významně ovlivňují výsledky psychofarmakologické léčby.
Zajímavý je dále vliv věku. Ve sledovaném souboru začala deprese u 38 % do 18 let, u zbývajících později. Skupina osob s časnou depresí byla charakterizována tím, že tyto osoby měly častěji rodinnou zátěž depresí, častěji se pokusily o sebevraždu, častěji se jednalo o ženy a měly méně komorbidních úzkostných poruch. Obě skupiny se ale nelišily ve výsledcích léčení. V jiném dělení kohorta osob s depresí ve věku nad 50 let měla častější depresivní epizody v minulosti, jejich začátek byl časnější a pacienti měli více tělesných onemocnění. Méně často udávali sebevražedné pokusy. Typickou poruchou spánku pro ně bylo častější noční a předčasné ranní probouzení a méně hypersomnie. Opět se nelišili v míře dosažených remisí.
V tak významném projektu nebylo možno nepojednat též nejzávažnější komplikaci depresivní poruchy – sebevražedné jednání. 142 probandů ze 4001 uvedlo, že v jejich příbuzenstvu se vyskytla dokonaná sebevražda. V jejich rodinné anamnéze pak byly častěji konstatovány velká depresivní porucha, bipolární afektivní porucha, nadužívání návykových látek. Zajímavé bylo, že tato podskupina nemocných neudávala sama častěji sebevražedné myšlenky ve srovnání s ostatními ze studie STAR*D. 16,5 % z celého vzorku uvedlo, že se sami dříve pokusili o sebevraždu. Signifikantně častěji se jednalo o pacienty se somatickými chorobami, s nadužíváním alkoholu či jiných návykových látek, s častějšími pracovními neschopnostmi. Začátek jejich afektivní poruchy byl významně – o 8,9 roku – časnější a v jejich anamnéze bylo více prodělaných depresivních epizod. I aktuálně udávali častěji sebevražedné myšlenky.
V poslední době byla věnována velká pozornost možnosti, že antidepresivní léčba sama o sobě může přispět k suicidální aktivitě léčeného. 1909 léčených na začátku STAR*D studie uvedlo, že mají sebevražedné myšlenky. Po první konzultaci 57 % z nich uvedlo zlepšení a 5 % zhoršení tohoto stavu. Při poslední konzultaci 74 % pociťovalo zlepšení, 4 % zhoršení. Z 1721 léčených, kteří na začátku studie netrpěli sebevražednými myšlenkami, 7 % uvedlo, že se tyto vyskytly po první návštěvě. Jednalo se o pacienty s nadužíváním návykových látek, s hlubokou depresí s melancholickými rysy. Na základě těchto zjištění se dá potvrdit nález, že tendence k sebevraždě jsou jedním ze základních příznaků depresivní poruchy, které se objevují a mizí v různých etapách této závažné nemoci. Antidepresivní léčba ve většině příznaků působí příznivě i na tuto oblast. Ale u všech – a zvláště u „těžších“ – pacientů musíme této potenciálně nejzávažnější komplikaci deprese a její léčbě věnovat maximální pozornost a po sebevražedných tendencích cíleně pátrat. V genetické části studie STAR*D bylo zjištěno, že některé polymorfismy genů kódujících centrální signální cesty relevantní pro vznik deprese, jako jsou CREB1 nebo GRIK2 a GRIA3, významně souvisí s objevením se suicidálních tendencí u léčených pacientů. Jistě by bylo optimální mít možnost tyto vlohy u našich pacientů předem testovat. Avšak zatím se jedná o výsledky předběžné, které v běžné klinické praxi nelze rutinně využívat.
Ve studii byla velká pozornost věnována také genetickým markerům potenciálně souvisejícím s výsledky léčení. U 1953 pacientů bylo typizováno 68 kandidátních genů se 768 polymorfismy. Byly nalezeny některé významné souvislosti, jejichž interpretace je zatím ne zcela jasná a jednoznačná. Např. geny kódující expresi 5HT2A receptorů významně souvisely s výsledky léčby. 79,9 % homozygotů pro alelu A na rs7997012 dosáhlo kladné klinické odpovědi na citalopram na rozdíl od 62,4 % homozygotů pro G alelu. Nebo kombinace určité dispozice genů kódujících 5HT2A receptory s genem GRIK4 odpovědným za expresi určitého typu glutamátových receptorů zvyšovala pravděpodobnost kladné klinické odpovědi na léčbu citalopramem o 23 %. V jiné části STAR*D studie pak bylo poukázáno na tu skutečnost, že genetická dispozice může také souviset s výskytem nežádoucích účinků léků. Jednalo se o polymorfismy genů kódujících expresi přenašeče serotoninu (HTTLPR). Zvýšené hladiny tohoto přenašeče mohou souviset s lepší snášenlivostí farmakologické léčby. Problémy této a dalších obdobných studií je, že při jejich replikaci nedojde k potvrzení předchozích výsledků. Tak tomu bylo i ve studii STAR*D, ve které nebyly např. potvrzeny předchozí nálezy významných vlivů genů fosfodiesterázy (PDE11A, 9A,1A) na výsledky antidepresivní léčby.
Je vhodné zdůraznit, že výsledky STAR*D studie, která probíhala v reálném světě běžných pacientů, jsou možná lepší, než se kterými se setkáváme v běžných praxích. Autoři v tomto směru poukazují na význam systematického měření výsledků léčby a léčebného postupu podle doporučených standardů týkajících se dávky léku, délky jeho podávání i jeho záměny či augmentace. Pojem „sequenced treatment measurement-based care“ – sekvenční léčba spojená s měřením výsledků – si budeme muset zapamatovat a hlavně podle něj postupovat i v naší praxi. I u nás máme k dispozici doporučené postupy jak pro praktické lékaře, tak pro specialisty a máme dostupné měřící škály, které je možné v praxi dobře použít. Rád bych jen doplnil, že každý léčebný postup musí být přísně individualizovaný s přihlédnutím ke všem faktorům biologickým i psychosociálním, které naši snahu, jak bylo uvedeno výše, bezpochyby ovlivňují.
Poučné je také zjištění, že uvedený systém léčby funguje nejen ve specializovaných ambulancích, ale také v zařízeních primární péče. Výsledky léčby psychiatry a praktickými lékaři se nelišily v žádném podstatném parametru. Kladné klinické odpovědi bylo dosaženo v prvním kroku u specialistů u 45,7 % léčených, u praktiků u 47,6 % pacientů, remise u 32,5 %, resp. 33,1 %. Čas do dosažení remise byl také prakticky stejný – 6,2, resp. 5,5 týdne.
Vzhledem k vysoké prevalenci afektivních poruch, jejich tendenci ke chronickému průběhu, zásadnímu narušení kvality života i pracovní schopnosti postiženého a z toho plynoucí invalidizaci i k možnému fatálnímu vyústění ve formě sebevraždy je včasná diagnostika a účinná léčba tohoto onemocnění zásadní. Výsledky studie STAR*D i jiných studií i naše klinické zkušenosti potvrzují, že současná medicína dokáže většině těchto nemocných velmi výrazně pomoci. Zlatým pravidlem léčby depresivní epizody je v současné době monoterapie jedním z moderních antidepresiv, event. v kombinaci s psychoterapií. Objevují se ale i nové otázky. Neměla by v některých předem specifikovaných případech být postupem první volby kombinovaná terapie více léky třeba i za použití dalších nových druhů psychofarmak (např. atypická antipsychotika, antiepileptika) nebo jiných psychoterapeutických metod? Připadalo by to do úvahy např. u mladých pacientů s první epizodou, u kterých je vysoká pravděpodobnost přerušení léčby, pakliže nezažijí časné zlepšení svého stavu. Jistě budou dále nalézány ukazatele jak biologického, tak psychopatologického nebo psychosociálního rázu, které nám v tomto směru mohou poskytnout pomoc. První kroky jsou již činěny v současné době i na našich pracovištích.
Podpořeno projekty MŠMT 1M 06039 a 0021620849.
Použité zkratky
cAMP – cyklický adenozinmonofosfát
CREB1 – gen kódující expresi proteinu vázajícího se v genomu na element odezvy na cAMP
GRIA3, GRIK2 – geny kódující expresi inotropních glutamátových receptorů
HAMD-17 – 17položková Hamiltonova škála pro depresi
HTTLPR – gen kódující expresi přenašeče serotoninu
IMAO – inhibitory monoaminooxidázy
KBT – kognitivně-behaviorální terapie
NaSSA – noradrenergní a specificky serotoninergní antidepresiva
NDRI – inhibitory zpětného vychytávání noradrenalinu a dopaminu
NIMH – Národní ústav pro duševní zdraví
USA QIDS-SR – sebeposuzující krátká škála pro depresivní symptomatiku
SNRI – inhibitory zpětného vychytávání serotoninu a noradrenalinu
SSRI – specifické inhibitory zpětného vychytávání serotoninu
STAR*D – studie sekvenční alternativy léčby deprese
TCA – tricyklická antidepresiva
O autorovi: Prof. MUDr. Jiří Raboch, DrSc. Univerzita Karlova v Praze, 1. lékařská fakulta a Všeobecná fakultní nemocnice, Psychiatrická klinika,
e-mail: raboch.jiri@vfn.cz

